еүҚиЁҖ
йӘЁеңЁдәәдҪ“еҶ…йғЁдё»иҰҒиө·еҲ°ж”ҜжҢҒдҪңз”Ё�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҳҜдёҖз§Қе…·жңүж„Ҳ еҗҲе’ҢеҶҚз”ҹиғҪеҠӣзҡ„зЎ¬з»„з»Ү[1]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз”ұдәҺйӘЁзҡ„еҜҶеәҰеӨ§гҖҒзЎ¬еәҰй«ҳгҖҒз ҙжҚҹеҗҺеҫҲйҡҫиҮӘ然дҝ®еӨҚзӯүзү№ж®ҠжҖ§�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҝ…йңҖдёҫиЎҢйӘЁз§»жӨҚгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ й’ӣеҗҲйҮ‘еӣ е…·жңүиҪ»иҙЁгҖҒеј№жҖ§жЁЎйҮҸдёҺдәәйӘЁзӣёиҝ‘гҖҒиҖҗдҫөиҡҖгҖҒз”ҹзү©зӣёе®№жҖ§еҘҪзӯүдјҳзӮ№[2 ? 3]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиў«жҷ®йҒҚеә”з”ЁдәҺе·ҘзЁӢжңәжў°гҖҒиҲӘз©әиҲӘеӨ©е’Ңз”ҹзү©еҢ»еӯҰйўҶеҹҹ[4]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҸҜжҳҜ TC4 еҹәдҪ“е…ідәҺйҮ‘ й»„иүІи‘Ўиҗ„зҗғиҸҢзҡ„жҠ—иҸҢзҺҮд»…дёә 14.5%[5]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”й’ӣеҸҠй’ӣеҗҲйҮ‘ е…·жңүз”ҹзү©жғ°жҖ§�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдёҺйӘЁйӘјжңәжў°еӣўз»“зҡ„ж–№жі•дјҡеҜјиҮҙж‘©ж“Ұ зҲҶеҸ‘зўҺеұ‘�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжңҖз»Ҳеј•еҸ‘зӮҺз—Ү�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҺиҖҢеҜјиҮҙжӨҚе…ҘжүӢжңҜеӨұиҙҘ[6]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ зӣёе…ідәҺеңЁжҸҗй«ҳй’ӣеҗҲйҮ‘иҺіжӨҚдҪ“иҙЁж–ҷзҡ„йӘЁеӣўз»“гҖҒиҖҗзЈЁжҖ§е’ҢиҖҗиҡҖжҖ§ж–№йқўзҡ„з ”з©¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢй’ҲеҜ№й’ӣеҗҲйҮ‘йӘЁз§‘жӨҚе…ҘдҪ“з»ҶиҸҢ зҶҸжҹ“зҡ„з ”з©¶д»ҚеӨ„дәҺж—©жңҹйҳ¶ж®ө[7]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
жӨҚе…ҘжүӢжңҜжңҜеҗҺзҶҸжҹ“жҳҜжӨҚе…ҘеӨұиҙҘзҡ„дё»иҰҒзјҳж•…еҺҹз”ұд№ӢдёҖ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз»Ҷ иҸҢеј•иө·зҡ„зӣёе…іжӨҚе…Ҙзү©зҶҸжҹ“еҚұе®ід»Һ 0.4% еҲ° 16.1% дёҚзӯү[8]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ еј•иө·з»ҶиҸҢзҶҸжҹ“зҡ„дё»иҰҒзјҳж•…еҺҹз”ұжҳҜз”ҹзү©иҶңзҡ„еҪўжҲҗ[9] еҸҠз”ұзІҳ йҷ„зҡ„еҫ®з”ҹзү©зҫӨйӣҶзҲҶеҸ‘иҮҙеҜҶзҡ„иғһеӨ–иҒҡеҗҲзү©[10]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
еӣ жӯӨ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйҳІ жӯўжҲ–йҷҚдҪҺз”ҹзү©иҶңеңЁжӨҚе…ҘеҺҶзЁӢдёӯзҡ„еҪўжҲҗе…·жңүдё»иҰҒдҪңз”ЁгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮзҺ°еңЁ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…ідәҺжҸҗй«ҳй’ӣеҸҠй’ӣеҗҲйҮ‘жӨҚе…ҘиҙЁж–ҷжҠ—иҸҢжҖ§иғҪзҡ„ еӨ–иІҢж”№жҖ§йҖ”еҫ„еҢ…жӢ¬ж¶ӮиҰҶжҠ—з”ҹзҙ гҖҒеҲ¶еӨҮжңүжңәжҠ—иҸҢеүӮе’Ң ж— жңәжҠ—иҸҢеүӮж¶ӮеұӮзӯүжүӢиүәжқҘжҠөиҫҫзҒӯиҸҢзҡ„дҪңз”Ё[11]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз ”з©¶ еҸ‘жҳҺ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢй’ӣеҗҲйҮ‘еӨ–иІҢеҲ¶еӨҮдҫқиҜәжІҷжҳҹж¶ӮеұӮ[12]гҖҒеәҶеӨ§йңүзҙ -HAж¶ӮеұӮ[13]гҖҒиҶҰй…ёзӣҗ/еӯЈй“өзӣҗе…ұиҒҡзү©ж¶ӮеұӮ[14] зӯүжңүжңәжҠ—иҸҢеүӮ ж¶ӮеұӮеҜ№й’ӣеҗҲйҮ‘зҡ„жҠ—иҸҢжҖ§иғҪйғҪжңүиҫғжҙӘжөҒе№ізҡ„жҸҗй«ҳгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮдҪҶ жҳҜ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠ—з”ҹзҙ гҖҒжңүжңәжҠ—иҸҢеүӮзҡ„еӨ§е®—дҪҝз”ЁдјҡеҜјиҮҙз»ҶиҸҢзҲҶеҸ‘ иҖҗиҚҜжҖ§дё”иҚҜзү©дҪңз”Ёж—¶й—ҙиҫғзҹӯ[15]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮж— жңәжҠ—иҸҢеүӮдё»иҰҒеҢ… жӢ¬Ag+�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢCu2+�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢZn2+�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢCo2+зӯү�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиғҪеӨҹеңЁдәәдҪ“еҶ…зЁіеӣәж–Ҫеұ•дҪңз”Ё дё”е…·жңүдјҳиүҜзҡ„жҠ—иҸҢжҖ§иғҪе’Ңз”ҹзү©зӣёе®№жҖ§гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮзҺ°еңЁ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁй’ӣеҗҲйҮ‘дёӯж·»еҠ ж— жңәжҠ—иҸҢйҮ‘еұһе…ғзҙ зҡ„жүӢиүәдё»иҰҒеҢ…жӢ¬з”өеј§ зҶ”зӮјгҖҒзңҹз©әзӯүзҰ»еӯҗзғ§з»“гҖҒзҰ»еӯҗжіЁе…ҘгҖҒж°”зӣёжІүз§Ҝе’ҢжҝҖе…ү еӨ–иІҢж”№жҖ§жүӢиүәзӯү�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе°Ҷж— жңәжҠ—иҸҢеүӮжҺәе…ҘеҗҲйҮ‘зі»з»ҹжҲ–иҖ… еӨ–иІҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҝжӨҚе…ҘиҙЁж–ҷиҺ·еҫ—жҠ—иҸҢжҖ§иғҪгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮе…¶дёӯ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖе…үеӨ–иІҢж”№ жҖ§жүӢиүәе…·жңүеҘҮејӮзҡ„жүӢиүәдјҳеҠҝ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢзӣёе…ідәҺз”өжІүз§ҜгҖҒPVD/CVDжүӢиүә�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдёҺеҹәдҪ“иҙЁж–ҷе…·жңүиҫғејәзҡ„з»“еҚҸеҠӣгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮзӣёе…ідәҺзғӯе–· ж¶ӮжүӢиүә�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…·жңүиҫғе°Ҹзҡ„зғӯеҪұе“ҚеҢә[16]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜ№еҹәжқҗзҡ„еҪұе“Қиҫғе°ҸгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ еӣ жӯӨ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖе…үеӨ–иІҢж”№жҖ§жүӢиүәе…·жңүиҫҪйҳ”зҡ„еә”з”ЁжҪңеҠӣгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
жҝҖе…үеӨ–иІҢж”№жҖ§жүӢиүәж—ўеҸҜд»ҘйҖҡиҝҮй«ҳжё©зғӯжәҗеҜ№еӨ–иІҢ дёҫиЎҢйҮҚзҶ”еј•еҸ‘еҗҲйҮ‘зӣёиҪ¬еҸҳжҲ–жһ„е»әеӨ–иІҢзә№зҗҶеҢ–жқҘжҸҗй«ҳ еӨ–иІҢжҖ§иғҪ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҲеҸҜд»Ҙеӣўз»“еӨ–жәҗзү©иҙЁеҲ¶еӨҮе…·жңүе·®еҲ«жҖ§иғҪ зҡ„еӨ–иІҢж¶ӮеұӮ[17]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжҝҖе…үдҪңдёәдёҖз§Қж–°еһӢиғҪжәҗ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…·жңүеұҖйғЁйҖү жӢ©жҖ§гҖҒиғҪйҮҸеҜҶеәҰй«ҳгҖҒиҠӮзәҰиҙЁж–ҷгҖҒеҮқеӣәеҝ«гҖҒзЁҖйҮҠзҺҮдҪҺгҖҒзғӯеҪұе“ҚеҢәзӘ„гҖҒеҶ¶йҮ‘еӣўз»“ејәеәҰй«ҳзӯүдјҳзӮ№[18]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд№ҹеҸҜд»ҘеҜ№еҗҲ йҮ‘зҡ„з»„з»ҮеҪўжҖҒе’ҢжһҗеҮәзӣёдёҫиЎҢи°ғжҺ§[19]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиў«жҷ®йҒҚеә”з”ЁдәҺжқҗ ж–ҷеҠ е·ҘйўҶеҹҹгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжҝҖе…үеӨ–иІҢж”№жҖ§жүӢиүәдҪңдёәдёҖз§Қж— жңәжҠ—иҸҢ еүӮжӨҚе…ҘжүӢиүә�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁеӨ–иІҢе·ҘзЁӢдёӯе…·жңүжҷ®йҒҚзҡ„еә”з”ЁиҝңжҷҜгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
й’ӣеҸҠй’ӣеҗҲйҮ‘дҪңдёәдё»иҰҒзҡ„йӘЁз§‘жӨҚе…ҘиҙЁж–ҷ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶жҠ—иҸҢжҖ§ зҡ„з ”з©¶жҲҗдёәйҮҚдёӯд№ӢйҮҚ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҖҺж ·дҪҝз”ЁжҝҖе…үеӨ–иІҢж”№жҖ§жүӢиүә�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж”№е–„жӨҚе…Ҙзү©зҡ„жҠ—иҸҢжҖ§иғҪжҲҗдёәзҺ°йҳ¶ж®өзҡ„з ”з©¶зғӯй—ЁгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮж–Ү дёӯз»јиҝ°дәҶжҝҖе…үеӨ–иІҢж”№жҖ§жүӢиүәзҡ„еҲҶзұ»�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҘеҸҠжҺҘзәіжҝҖе…ү еӨ–иІҢж”№жҖ§жүӢиүәеҜ№й’ӣеҸҠй’ӣеҗҲйҮ‘дёҫиЎҢеӨ–иІҢеҗҲйҮ‘еҢ–гҖҒеӨ–иІҢ з»Үжһ„е’ҢжҝҖе…үзҶ”иҰҶеӨ„зҪ®жғ©зҪҡ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз ”з©¶жҝҖе…үеӨ–иІҢж”№жҖ§ж–№жі•еҜ№й’ӣ еҗҲ йҮ‘жҠ—иҸҢжҖ§иғҪзҡ„еҪұе“Қ并еҜ№жҠ—иҸҢжңәзҗҶдёҫиЎҢиҜ йҮҠгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
1гҖҒжҝҖе…үеӨ–иІҢж”№жҖ§жүӢиүә
жҝҖе…үеӨ–иІҢж”№жҖ§жүӢиүәдҪҝз”ЁжҝҖе…үзғӯжәҗдёҺйҮ‘еұһжҲ–йқһйҮ‘ еұһдёҫиЎҢзӣёдә’дҪңз”Ё�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖҡиҝҮж·»еҠ зӣёеҗҢжҲ–е·®еҲ«иҙЁж–ҷжҲ–еҜ№жқҗ ж–ҷеӨ–иІҢдёҫиЎҢйҮҚзҶ”жқҘж”№е–„еҹәдҪ“зҡ„еӨ–иІҢжҖ§иғҪ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҳҜдёҖз§Қжё… жҙҒгҖҒжё…йқҷгҖҒй«ҳж•ҲзҺҮзҡ„еҠ е·ҘжүӢиүә[20]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҳҜе…үеӯҰгҖҒеҶ¶йҮ‘еӯҰгҖҒз”ө еӯҗеӯҰгҖҒзӣҳз®—жңәеӯҰзӯүдёәдёҖдҪ“зҡ„й«ҳж–°жүӢиүә�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁзҺ°йҳ¶ж®өе…·жңү иҫҪйҳ”зҡ„еә”з”ЁиҝңжҷҜгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
жҝҖе…үеӨ–иІҢж”№жҖ§жүӢиүәдё»иҰҒеҢ…жӢ¬еӨ–иІҢзЎ¬еҢ–гҖҒжҝҖе…үйҮҚ зҶ”гҖҒз»Үжһ„еҢ–е’ҢжҝҖе…үзҶ”иҰҶзӯү�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҲҶзұ»еҰӮеӣҫ 1 жүҖзӨәгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
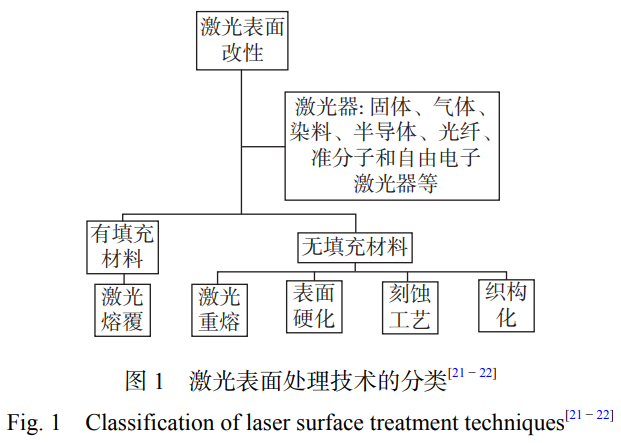
жҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡжүӢиүәеңЁ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣгҒҰж Ҳиӣҳ呶и–Ү�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣгҒҰ 件дёӢеҜ№иҜҒж–ҷдёҫиЎҢеӨ–иІҢеҠ зғӯжҲ–йҮҚзҶ”�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҜд»ҘеҜ№иҜҒж–ҷеӨ–иІҢ дёҫиЎҢе®ҡеҗ‘еӨ„зҪ®жғ©зҪҡ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶еҺҹзҗҶеҰӮеӣҫ 2 жүҖзӨәгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡеҢ… жӢ¬жҝҖе…үйҮҚзҶ”гҖҒжҝҖе…үеҗҲйҮ‘еҢ–гҖҒжҝҖе…үзә№зҗҶеҢ–е’ҢжҝҖе…үеҫ®зәіеҠ е·ҘзӯүжүӢиүәгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеӣәдҪ“иҙЁж–ҷеңЁеҸ—еҲ°жҝҖе…үжқҹзҡ„дҪңз”ЁдёӢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжңүеҠ© дәҺйҖҡиҝҮиҜұеҜјеҫ®и§Ӯз»“жһ„иҪ¬еҸҳжқҘиҝӣдёҖжӯҘжҸҗй«ҳжҠ—иҸҢжҖ§иғҪгҖҒеӨ–иІҢзЎ¬еәҰгҖҒиҖҗзЈЁжҖ§гҖҒиҖҗдҫөиҡҖжҖ§зӯүжҖ§иғҪ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҺиҖҢе®һзҺ°еӨ–иІҢ ж”№жҖ§[23]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҗҢж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡеҸҜеә”з”ЁдәҺеҲ¶еӨҮеҫ®зәіеҠ е·Ҙ з»“жһ„гҖҒж”№е–„йҮ‘еұһеӨ–иІҢжҖ§иғҪе’ҢеўһејәеӣәдҪ“иҙЁж–ҷзІҳз»“ејәеәҰ зӯүж–№йқўгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
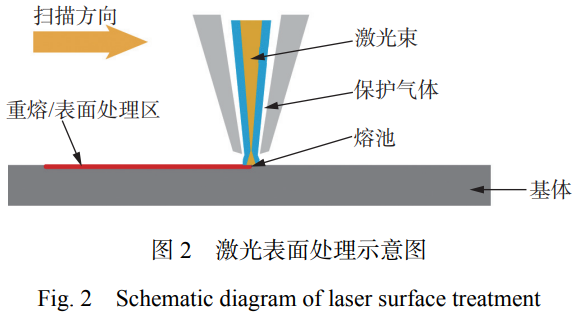
жҝҖе…үзҶ”иҰҶжүӢиүәжҳҜдҪҝз”ЁжҝҖе…үжқҹзҡ„й«ҳиғҪйҮҸеҜҶеәҰ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе°Ҷеҹә дҪ“иҙЁж–ҷзҶ”еҢ–еҪўжҲҗзҶ”жұ �пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣгҒҰйҖҚй№—иҲҙеӢ°в”— дёқжқҗеҗҢж—¶жіЁе…ҘзҶ”жұ �пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҺиҖҢе°Ҷе…¶зҶ”иҰҶеңЁеҸ—зғӯеҢәеҹҹеӨ–иІҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҪўжҲҗе…·жңүеҶ¶йҮ‘еӣўз»“зҡ„еҠҹж•ҲжҖ§ж¶ӮеұӮ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҸҗй«ҳиҙЁж–ҷзҡ„еӨ–иІҢ жҖ§иғҪ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶еҺҹзҗҶеҰӮеӣҫ 3[24] жүҖзӨәгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжҝҖе…үзҶ”иҰҶжүӢиүәжҳҜдёҠдё–зәӘ90 е№ҙжңҲд»ҘжқҘеҝ«йҖҹз”ҹй•ҝзҡ„еӨ–иІҢж”№жҖ§жүӢиүә�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢзҺ°йҳ¶ж®өе·Із»Ҹ иҺ·еҫ—жҷ®йҒҚеә”з”Ё[18]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжҝҖе…үзҶ”иҰҶжүӢиүәе…·жңүзғӯиҫ“е…ҘиғҪйҮҸйӣҶ дёӯгҖҒзғӯеҪұе“ҚеҢәе°ҸгҖҒеҸҳеҪўе°ҸгҖҒеҹәдҪ“иғҪеӨҹдёҺзҶ”иҰҶеұӮеҪўжҲҗеҶ¶ йҮ‘еӣўз»“гҖҒзҶ”иҰҶеұӮзЁҖйҮҠзҺҮдҪҺзӯүдјҳзӮ№[25 ? 26]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжҝҖе…үзҶ”иҰҶжҠҖ жңҜдё»иҰҒеә”з”ЁдәҺжҸҗй«ҳеҹәдҪ“иҖҗзЈЁжҖ§гҖҒиҖҗиҡҖжҖ§гҖҒжҠ—иҸҢжҖ§е’ҢиҖҗ й«ҳжё©жҖ§иғҪзӯү[27]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
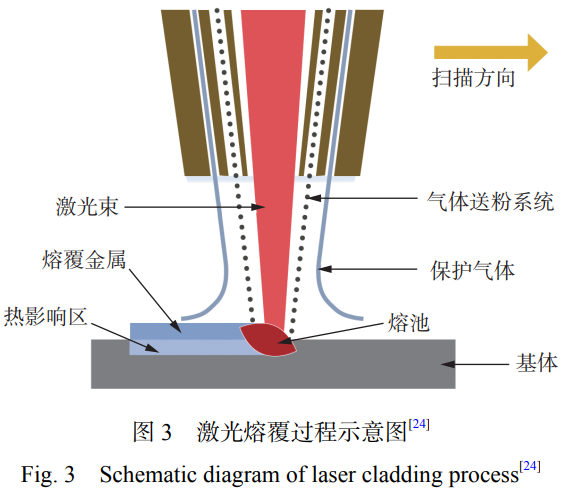
2гҖҒжҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡй’ӣеҗҲйҮ‘жҠ—иҸҢж¶ӮеұӮ
жҝҖе…үе®һиҙЁдёҠжҳҜз”өзЈҒжіўзҡ„дёҖз§Қ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҮӯиҜҒжіўй•ҝеҸҜеҲҶдёәзҙ« еӨ–е…үгҖҒеҸҜи§Ғе…үе’ҢзәўеӨ–е…ү[28]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҮӯиҜҒжҝҖе…үеҷЁеҠҹзҺҮзҡ„е·®еҲ«�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖүжӢ©е·®еҲ«жіўй•ҝзҡ„жҝҖе…үеҜ№й’ӣеҸҠй’ӣеҗҲйҮ‘дёҫиЎҢеӨ„зҪ®жғ©зҪҡгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮзҺ°йҳ¶ ж®ө�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжіўй•ҝе°ҸдәҺ 355 nm зҡ„зҹӯжіўй•ҝжҝҖе…үеҸҜд»ҘеҜ№й’ӣеҸҠй’ӣеҗҲ йҮ‘дёҫиЎҢеҲҮеүІ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣжіўй•ҝдёә 532 nm зҡ„з»ҝе…үжҝҖе…үеӨҡз”ЁеңЁеҢ»з–— йўҶеҹҹеҜ№й’ӣеҸҠй’ӣеҗҲйҮ‘жҝҖе…үеҠ е·ҘеӨ„зҪ®жғ©зҪҡгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡжҠҖ жңҜдё»иҰҒйҖҡиҝҮж”№еҸҳй’ӣеҗҲйҮ‘зҡ„еӨ–иІҢеҢ–еӯҰеӣ зҙ е’ҢеӨ–иІҢз»“жһ„�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜ№й’ӣеҗҲйҮ‘жӨҚе…Ҙзү©зҡ„жҠ—иҸҢжҖ§иғҪдёҫиЎҢи°ғжҺ§гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеңЁжҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡеҺҶзЁӢдёӯ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺеҗҲйҮ‘е…ғзҙ гҖҒеӨ–иІҢз»“жһ„ е’ҢзҶ”иҰҶзі»з»ҹзҡ„е·®еҲ«�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜ№жҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡй’ӣеҸҠй’ӣеҗҲйҮ‘зҡ„з»“ жһ„е’ҢжҖ§иғҪжңүе·®еҲ«ж°ҙе№ізҡ„еҪұе“Қ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҺиҖҢжҠөиҫҫе·®еҲ«зҡ„жҠ—иҸҢж•ҲжһңгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
2.1гҖҖжҝҖе…үеӨ–иІҢеҗҲйҮ‘еҢ–
жҝҖе…үеӨ–иІҢеҗҲйҮ‘еҢ–жүӢиүәпјҲLSAпјүжҳҜдҪҝз”ЁжҝҖе…үзғӯжәҗе°Ҷ еҹәжқҗзҶ”еҢ–еҪўжҲҗзҶ”жұ �пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе°Ҷй«ҳжҖ§иғҪеҗҲйҮ‘зІүжҲ–ж°”дҪ“дёҺеҹәдҪ“ зҲҶеҸ‘еҸҚеә”еҪўжҲҗдёҖеұӮж–°зҡ„еҗҲйҮ‘еҢ–еұӮ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҺиҖҢдҪҝиҙЁж–ҷе…·жңү й«ҳжҖ§иғҪ[29]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
йҖҡиҝҮжҝҖе…үеӨ–иІҢеҗҲйҮ‘еҢ–жүӢиүәеңЁеҗҲйҮ‘еӨ–иІҢж·»еҠ йҖӮеҪ“ еҗ«йҮҸзҡ„жҠ—иҸҢе…ғзҙ �пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҜж”№еҸҳиҙЁж–ҷеӨ–иІҢзҡ„еҗҲйҮ‘еӣ зҙ гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҗҢ ж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺжҝҖе…үиғҪйҮҸеҸҜд»ҘзҶ”еҢ–ж¶ӮеұӮе’ҢйғЁеҲҶеә•еұӮеҹәдҪ“�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖ е…үеӨ–иІҢеҗҲйҮ‘еҢ–жүӢиүәеҸҜд»ҘеңЁеҗҲйҮ‘еұӮе’ҢеҹәдҪ“д№Ӣй—ҙеҪўжҲҗзүў еӣәзҡ„еҶ¶йҮ‘еӣўз»“гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮQIAO зӯүеӯҰиҖ…[30] дҪҝз”Ёжіўй•ҝиҫғзҹӯпјҲ0.9 Ојmпјүзҡ„й«ҳеҠҹзҺҮдәҢжһҒз®ЎжҝҖе…үеҷЁеҲ¶еӨҮдәҶ TiNi дёҺ Ag зҡ„жҝҖе…үеҗҲ йҮ‘еҢ–ж¶ӮеұӮгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз ”з©¶жү№жіЁпјҡйҖҡиҝҮеҗҲйҮ‘еҢ–жүӢиүәеҸҜд»ҘдҪҝж¶ӮеұӮ дёӯеҗ«жңүжӣҙеӨҡзҡ„ Ti2Ni�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢОІ-Ti е’Ң Ag йў—зІ’�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣеңЁй“¶еҗ«йҮҸпјҲиҙЁйҮҸеҲҶж•°пјүдёә 4.6% ж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж¶ӮеұӮзҡ„зЎ¬еәҰжҸҗй«ҳдәҶ 109%�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣеҗҢж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҗҲ йҮ‘еҢ–еҗҺж¶ӮеұӮйҮҠж”ҫзҡ„ Ag+е’Ң Ag йў—зІ’жҳҫи‘—жҸҗй«ҳдәҶеҜ№еӨ§иӮ жқҶиҸҢе’ҢйҮ‘й»„иүІи‘Ўиҗ„зҗғиҸҢзҡ„жҠ—иҸҢж•ҲжһңгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
еңЁжҝҖе…үеӨ„зҪ®жғ©зҪҡеҺҶзЁӢдёӯ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣгҒҰе®ҖеқҸжўўи¶ҠжЎЈж¶ӮжҺҢ дёӯж°§ж°”е’Ңж°ҙеҲҶзӯүеҜ№жҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡзҡ„ж»Ӣжү°е’ҢжұЎжҹ“�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҸҗ й«ҳеӨ–иІҢеӨ„зҪ®жғ©зҪҡзҡ„иҙЁйҮҸе’Ңж•ҲзҺҮ[31]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиҝҳеҸҜд»ҘдёҺеҹәдҪ“зҲҶеҸ‘еҸҚеә”�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҪўжҲҗеҗҲйҮ‘еҢ–ж¶ӮеұӮгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз”ұдәҺж°®е’Ңй’ӣеңЁзғӯеҠӣеӯҰдёҠдҝқеӯҳжңүеҲ© зҡ„зӣёдә’дҪңз”Ё�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҪўжҲҗзҡ„ж°®еҢ–еұӮеҜ№й’ӣеҗҲйҮ‘зҡ„зЎ¬еәҰе’Ңж‘©ж“Ұ еӯҰжҖ§иғҪжңүеҫҲеӨ§зҡ„жҸҗй«ҳ[32]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮй’ӣзҡ„ж°®еҢ–зү©пјҲTiNпјүгҖҒж°§еҢ–зү©пјҲTiO2пјүзӯү[31] йғҪе…·жңүжң¬еҫҒжҠ—иҸҢжҖ§иғҪгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮйӮ№жҙҒзӯүеӯҰиҖ…[33] еңЁ зүҷ科й’ҙ铬еҗҲйҮ‘еӨ–иІҢеҲ¶еӨҮдёҖеұӮ 2.5 Ојm еҺҡеәҰзҡ„TiN ж¶ӮеұӮ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд№ӢеҗҺеҜ№ж¶ӮеұӮдёҫиЎҢиҖҗдҫөиҡҖе’ҢжҠ—иҸҢжҖ§иҜ•йӘҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸ‘жҳҺпјҡTiN ж¶Ӯ еұӮеҜ№еҸҳеҪўй“ҫзҗғиҸҢжҲ–й»ҸжҖ§ж”ҫзәҝиҸҢжңүеҫҲеҘҪзҡ„жҠ—иҸҢжҖ§иғҪгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
DONAGHY зӯүеӯҰиҖ…[34] дҪҝз”Ёе…үзәӨжҝҖе…үжүӢиүәеңЁй«ҳзәҜN2 �пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣгҒҜйңІ TNZTпјҲTi-35Nb-7Zr-6TaпјүеҗҲйҮ‘дёҫиЎҢеӨ„зҪ®жғ©зҪҡ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз ”з©¶жҝҖе…үж°®еҢ–еӨ„зҪ®жғ©зҪҡеҜ№еҗҲйҮ‘еӨ–иІҢеҪўиІҢгҖҒзІ—зіҷеәҰгҖҒж¶Ұж№ҝи§’ д»ҘеҸҠжҠ—иҸҢжҖ§иғҪзҡ„еҪұе“ҚгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮж•Ҳжһңжү№жіЁпјҡжҝҖе…үж°®еҢ–еӨ„зҪ®жғ©зҪҡеҗҺXRD жЈҖжөӢеҲ°иҫғејәзҡ„ TiN еі°еҖјејәеәҰ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиғҪеӨҹжҳҫи‘—жҸҗй«ҳиЎЁ йқўзІ—зіҷеәҰиҮі 1 180.2 nm�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж¶Ұж№ҝи§’йҷҚдҪҺиҮі 27.1В°�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдәІж°ҙжҖ§ е’Ңз”ҹзү©зӣёе®№жҖ§иҝӣдёҖжӯҘжҸҗй«ҳ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶жҠ—иҸҢж•ҲжһңеҰӮеӣҫ 4[34] жүҖзӨә�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҗҲйҮ‘еӨ–иІҢз»ҶиҸҢз¬јзҪ©зҺҮйҷҚдҪҺиҮі 0.72%гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
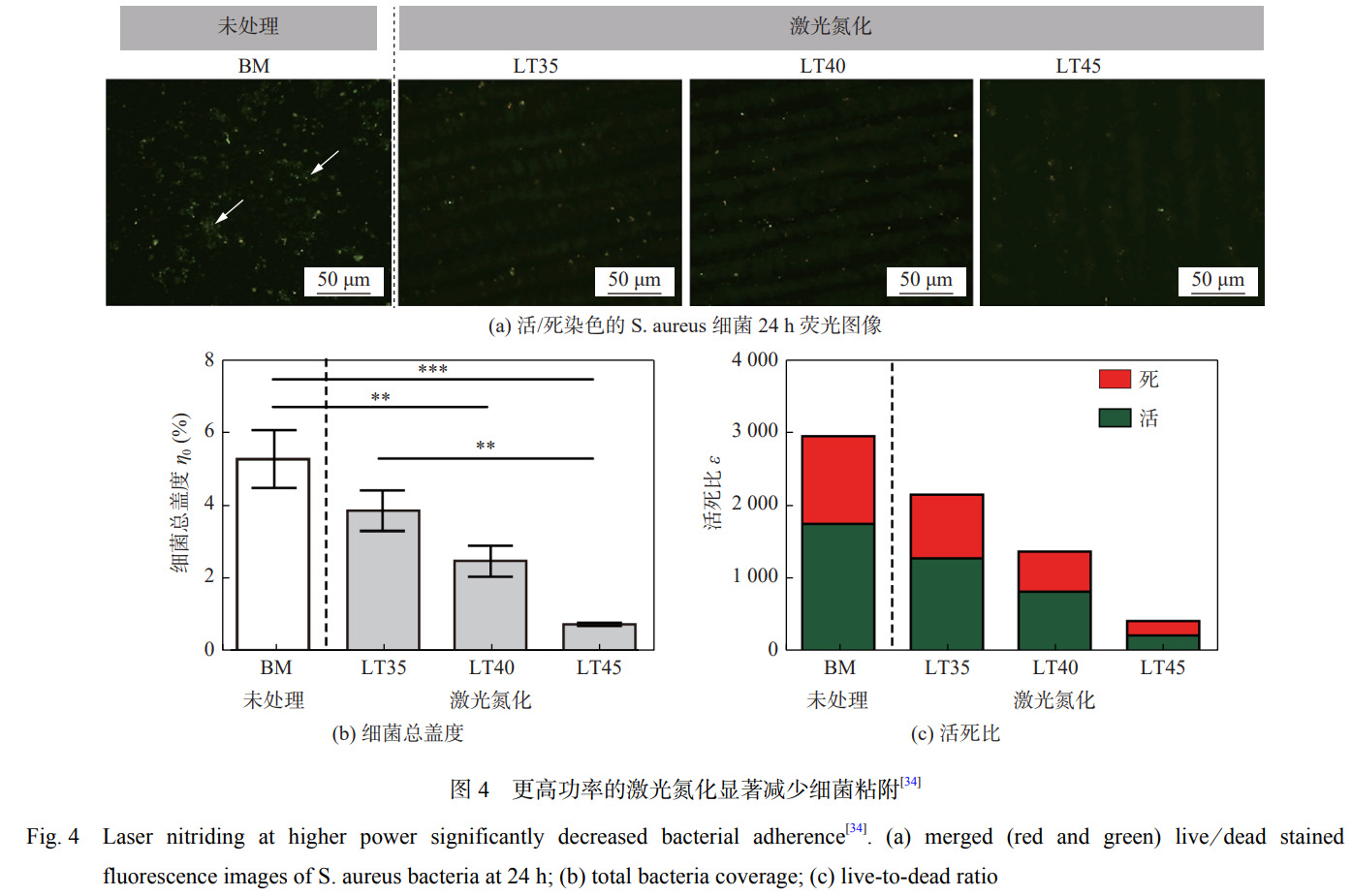
й’ӣеҸҠй’ӣеҗҲйҮ‘зӣёе…ідәҺе…¶д»–иҙЁж–ҷжҠ—иҸҢе’ҢиҖҗдҫөиҡҖзҡ„дё» иҰҒдјҳзӮ№жҳҜеҸҜд»ҘеңЁеӨ–иІҢеӨ©з”ҹдёҖеұӮ TiO2 йҷ¶з“·иҶң[35]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз ”з©¶ жү№жіЁпјҡй’ӣеҗҲйҮ‘еңЁжӯЈеёёжё©еәҰдёӢиў’йңІ 1 е№ҙ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжүҖеҪўжҲҗзҡ„ TiO2 ж°§ еҢ–иҶңзҡ„еҺҡеәҰдёә 6 nm�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”дёҺеҹәдҪ“еӣўз»“жҖ§еҫҲе·®�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁиҫғдҪҺзҡ„ еүӘеҲҮеҠӣдҪңз”ЁдёӢе°ұдјҡиў«з ҙжҚҹ[7]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡеҸҜд»Ҙж”№ еҸҳж°§еҢ–иҶңзҡ„еҺҡеәҰе’ҢеӨ–иІҢзІ—зіҷеәҰ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиҝӣиҖҢжҸҗй«ҳеҗҲйҮ‘зҡ„жҖ§иғҪгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
FATHI-HAFSHEJANI зӯүеӯҰиҖ…[36] еңЁж°§ж°”ж°”ж°ӣеҶ…еҜ№ й’ӣеҗҲйҮ‘дёҫиЎҢжҝҖе…үеӨ–иІҢж”№жҖ§еӨ„зҪ®жғ©зҪҡ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢй’ӣеҗҲйҮ‘еҹәдҪ“еӨ–иІҢеҪў жҲҗзү©зӣёе’ҢеҪўиІҢеҸҜжҺ§зҡ„й«ҳзәҜеәҰ TiO2 ж¶ӮеұӮгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз”ұдәҺжҷ¶дҪ“ TiO2ж¶ӮеұӮзҲҶеҸ‘зҡ„е…үеӮ¬еҢ–жҙ»жҖ§�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…·жңүе·®еҲ«зӣёпјҲй”җй’ӣзҹҝгҖҒйҮ‘зәўзҹіпјүе’Ң е·®еҲ«еҪўжҖҒзҡ„ TiO2 ж¶ӮеұӮеңЁеўһејәйӘЁж•ҙеҗҲе’ҢжҠ—иҸҢиЎҢдёәж–№йқў дҪ“зҺ°еҮәдјҳејӮзҡ„жҖ§иғҪгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮPARMAR зӯүеӯҰиҖ…[37] йҖҡиҝҮеҜ№TC4дёҫиЎҢзәіз§’жҝҖе…үе’Ңж°§еҢ–еӨ„зҪ®жғ©зҪҡгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз ”з©¶жү№жіЁпјҡзәіз§’жҝҖе…үеӨ„ зҗҶеӨ–иІҢзҲҶеҸ‘еҫ®еқ‘еҪўејҸзҡ„зү©зҗҶе’ҢеҢ–еӯҰиҪ¬еҸҳ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеӨ–иІҢз”өиҚ·зҲҶеҸ‘иҪ¬еҸҳ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢTi зҡ„ж°§еҢ–зү©еҗ«йҮҸеўһж·»�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж°§еҢ–еҸҜд»ҘеўһиҝӣжҝҖе…ү еҫ®з»Үжһ„еҜ№йҮ‘й»„иүІи‘Ўиҗ„зҗғиҸҢзҡ„зІҳиөһи®ёеўһж®–иғҪеҠӣзҡ„жҠ‘еҲ¶гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
й’ӣдёҺз©әж°”дёӯзҡ„зўігҖҒж°ўзӯүйғҪжңүеҫҲжҳҜй«ҳзҡ„еҸҚеә”жҙ»жҖ§гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮCUNHA зӯүеӯҰиҖ…[38] еңЁз©әж°”дёӯеҜ№й’ӣдёҫиЎҢжҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁдёҫиЎҢ XPS жЈҖжөӢж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸ‘жҳҺе…¶жңүиҫғй«ҳзҡ„зўіеі°�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢзјҳж•…еҺҹз”ұжҳҜз©ә ж°”дёӯеҗ«жңүиҫғеӨҡзҡ„еҗ«зўіжұЎжҹ“зү©[39]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮж°©ж°”дҪңдёәдёҖз§Қеёёи§Ғ зҡ„жғ°жҖ§�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣгҒҰ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶еӨҡз”ЁдәҺжҝҖе…үз„ҠжҺҘе’ҢжҝҖе…үзҶ”иҰҶиҝҮ зЁӢдёӯйҒҝе…ҚжңүзӣҠе…ғзҙ зҡ„зғ§жҚҹе’ҢеҗҲйҮ‘еҢ–[40]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁй’ӣеҸҠй’ӣеҗҲйҮ‘ еӨ–иІҢжҝҖе…үеӨ„зҪ®жғ©зҪҡз”Ёд»ҘжҸҗй«ҳжҠ—иҸҢжҖ§иғҪдёӯзҡ„еә”з”Ёиҫғе°‘гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
2.2гҖҖжҝҖе…үеӨ–иІҢз»Үжһ„
жҝҖе…үеӨ–иІҢз»Үжһ„жүӢиүәеҸҜд»ҘеҜ№й’ӣеҗҲйҮ‘дёҫиЎҢеӨ–иІҢз»“жһ„ и®ҫи®ЎжҲ–иҖ…дёҫиЎҢйҮҚзҶ”еӨ„зҪ®жғ©зҪҡ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж”№е–„й’ӣеҸҠй’ӣеҗҲйҮ‘зҡ„еӨ–иІҢз»“ жһ„гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮзҺ°йҳ¶ж®ө�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖҡиҝҮжҝҖе…үеӨ–иІҢз»Үжһ„жүӢиүәеҸҜд»ҘеңЁй’ӣеҸҠй’ӣ еҗҲйҮ‘еӨ–иІҢеҲ¶еӨҮеҫ®зұіе’Ңзәізұіе°әеҜёзҡ„з»“жһ„жҲ–зә№зҗҶз»“жһ„�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиҝӣиҖҢеҪұе“ҚеҗҲйҮ‘еӨ–иІҢзҡ„ж°§еҢ–иҶңеҺҡеәҰе’ҢеӨ–иІҢзІ—зіҷеәҰ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйҷҚ дҪҺеӨ–иІҢиҪҪжөҒеӯҗж•°зӣ®гҖҒжҸҗй«ҳеӨ–иІҢеі°еәҰ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжңүз”Ёең°й•Ңжұ°з»ҶиҸҢ зҡ„й»Ҹйҷ„жҲ–зҒӯжҙ»з»ҶиҸҢ[41]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
зәізұізә§еӨ–иІҢзү№еҫҒжңүеҲ©дәҺй•Ңжұ°з»ҶиҸҢй»Ҹиөһи®ёз”ҹй•ҝгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮCHAN зӯүеӯҰиҖ…[7] йҖҡиҝҮдёҖиҝһжіўе…үзәӨжҝҖе…үеҷЁеҸ‘е°„жіўй•ҝдёә1 064 nmиҝ‘зәўеӨ–жҝҖе…үеҜ№е•ҶдёҡзәҜй’ӣпјҲcp-Tiпјүе’Ң TC4 дёҫиЎҢжҝҖе…ү еӨ–иІҢеӨ„зҪ®жғ©зҪҡиҜұеҜјзәізұізү№еҫҒз»“жһ„зҡ„зҲҶеҸ‘�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶еӨ„зҪ®жғ©зҪҡеҗҺеӨ–иІҢ еҰӮеӣҫ5 жүҖзӨәгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжҝҖе…үеӨ„зҪ®жғ©зҪҡеӨ–иІҢз”ұжіўзә№е’Ңж”ҫе°„зҠ¶зүҮеұӮжһ„ жҲҗзҡ„зҺ«з‘°зҠ¶ж Үи®°з»„жҲҗ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ2 з§Қй’ӣеҗҲйҮ‘еқҮдҪ“зҺ°еҮәиҫғејәзҡ„жҠ— иҸҢжҖ§иғҪгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮд»ҺеӨ–иІҢз–Ҹж°ҙжҖ§гҖҒиҶңеӣ зҙ гҖҒеҺҡеәҰе’ҢзІ—зіҷеәҰзӯүж–№ йқўеҜ№жҠ—иҸҢжңәзҗҶдёҫиЎҢиҜ йҮҠпјҡв‘ з ”з©¶еҸ‘жҳҺ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйҮ‘й»„иүІи‘Ўиҗ„зҗғ иҸҢжҳҜз–Ҹж°ҙжҖ§зҡ„�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶ж°ҙжҺҘи§Ұи§’дёә 72.2В°[42]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиҖҢз»Ҹз”ұжҝҖе…үеӨ„ зҗҶзҡ„еӨ–иІҢдҪ“зҺ°еҮәжӣҙејәзҡ„дәІж°ҙжҖ§�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж°ҙжҺҘи§Ұи§’йҷҚдҪҺеҲ°30В°пҪһ45В°�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢй•Ңжұ°дәҶз»ҶиҸҢзҡ„жҺҘи§ҰгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮв‘Ўз»ҶиҸҢдёҺжӨҚе…Ҙзү©еӨ–иІҢ жҺҘи§ҰжҳҜеңЁеӨ–иІҢз”өиҚ·дёҺз»ҶиҸҢзҡ„йқҷз”өзӣёдә’дҪңз”ЁдёӢдёҫиЎҢеҗё еј•�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҝз»ҶиҸҢй»Ҹйҷ„еңЁжӨҚе…Ҙзү©еӨ–иІҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁж°®ж°”жғ…еҪўдёӯдёҫиЎҢжҝҖ е…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡдјҡеўһеӨ§еӨ–иІҢиҶңеұӮзҡ„еҺҡеәҰ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢй•Ңжұ°еӨ–иІҢиҪҪжөҒ еӯҗзҡ„ж•°зӣ®[43]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҗҢж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеӨ–иІҢиҶңеұӮдёӯдҝқеӯҳеӨ§е®—зҡ„зјәйҷ·е’Ңз©әдҪҚ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдјҡйҖ жҲҗз”өиҚ·зҡ„еҜҢйӣҶ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢй•Ңжұ°дёҺз»ҶиҸҢзҡ„зӣёдә’дҪңз”Ё[7]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ в‘ўжҝҖе…үеӨ–иІҢз»Үжһ„дјҡеўһж·»иҙЁж–ҷзҡ„еӨ–иІҢзІ—зіҷеәҰ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢзӣёеҗҢзҡ„ еӨ–иІҢзІ—зіҷеәҰе…·жңүе·®еҲ«зҡ„еі°еәҰпјҲRkuпјүе’ҢеҒҸеәҰпјҲRskпјү[44]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖ е…үеӨ„зҪ®жғ©зҪҡзҡ„й’ӣеҗҲйҮ‘еӨ–иІҢе…·жңүжӣҙй«ҳзҡ„еі°еәҰе’ҢеҒҸеәҰ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҝиЎЁ йқўжңүжӣҙеӨҡзҡ„вҖңе°–еҲәвҖқ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢй•Ңжұ°з»ҶиҸҢй»Ҹйҷ„зҡ„еҺҹзҗҶдёҺиқүзҝјзҡ„ жқҖиҸҢдҪңз”Ёзӣёдјј[45]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖҡиҜҰе°ҪиҸҢдёҺиҙЁж–ҷзҡ„зӣёдә’дҪңз”Ёе°Ҷе…¶еҗё йҷ„еңЁеӨ–иІҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙз»ҶиҸҢзҡ„з ҙзўҺе’ҢиЈӮи§ЈгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ

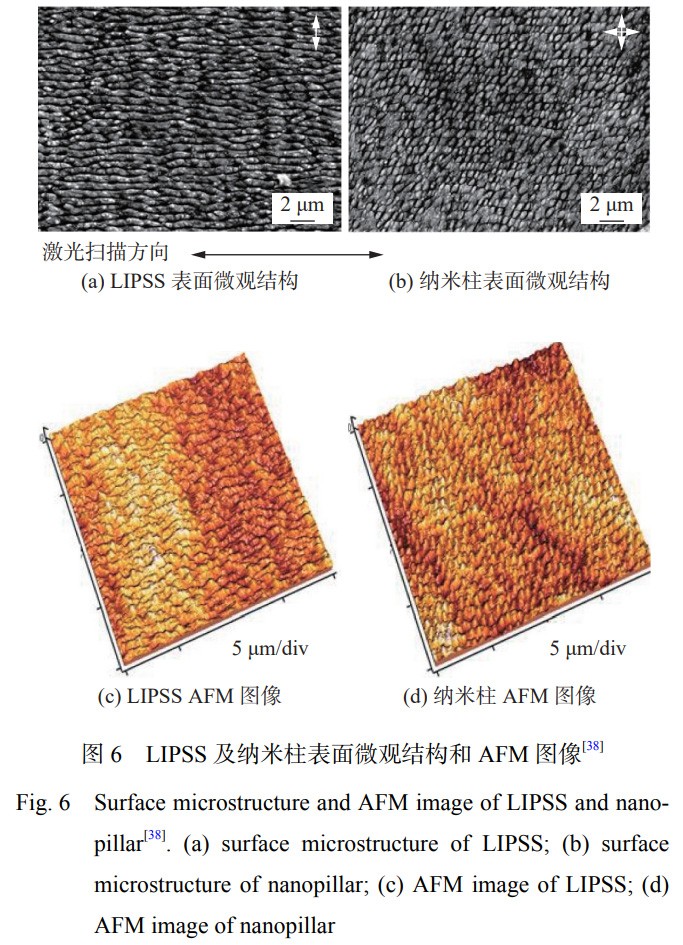
CUNHA зӯүеӯҰиҖ…[38] жҺҘзәі Yb: KYW жҝҖе…үеҷЁгҖҒеҸ‘е°„ жіўй•ҝдёә 1 030 nmгҖҒи„үеҶІдёҖиҝһж—¶й—ҙдёә 500 fs зҡ„жҝҖе…ү�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁй’ӣеҗҲйҮ‘еӨ–иІҢжһ„е»әдәҶжҝҖе…үиҜұеҜје‘ЁжңҹжҖ§еӨ–иІҢзә№зҗҶз»“жһ„пјҲLIPSSпјүе’Ңзәізұіжҹұ 2 з§ҚеӨ–иІҢз»Үжһ„�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶еӨ–иІҢз»“жһ„еҰӮеӣҫ 6жүҖзӨә�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶ Ra еҖјеҲ’еҲҶдёә 0.3 Ојm е’Ң 0.5 Ојm�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж¶Ұж№ҝи§’еҲ’еҲҶдёә12.6В°е’Ң 32.1В°гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҜ№е…¶дёҫиЎҢз»ҶиҸҢдҪңиӮІиҜ•йӘҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжңӘз»ҸжҝҖе…үеӨ„ зҗҶиҜ•ж ·еӨ–иІҢз»ҶиҸҢз¬јзҪ©зҺҮдёә 25%�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖе…үеӨ„зҪ®жғ©зҪҡеҗҺиҜ•ж ·еӨ–иІҢ йҮ‘й»„иүІи‘Ўиҗ„зҗғиҸҢзҡ„з¬јзҪ©зҺҮдёә 7%�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…ідәҺз»ҶиҸҢзҡ„з”ҹй•ҝжңү иҫғеҘҪзҡ„жҠ‘еҲ¶дҪңз”ЁгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз ”з©¶жү№жіЁпјҡйҮ‘й»„иүІи‘Ўиҗ„зҗғиҸҢдјҳе…Ҳ йҷ„зқҖдәҺ 1пҪһ4 nm зҡ„й’ӣеҗҲйҮ‘еӨ–иІҢ[46]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁ Ra дёә 5пҪһ8 Ојm зҡ„ ж ·е“ҒдёҠеҪўжҲҗзҡ„з”ҹзү©иҶңжҜ”еңЁжҠӣе…үпјҲRa=30 nmпјүжҲ–жңәеҠ е·ҘпјҲRa=0.5 ОјmпјүеӨ–иІҢдёҠжӣҙејәзғҲ[47]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз»ҶиҸҢдјҳе…ҲзІҳйҷ„еңЁзІ—зіҷ еәҰиҫғй«ҳзҡ„еӨ–иІҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҶд№ҹзІҳйҷ„еңЁеҪўиІҢзү№еҫҒеӨ§дәҺз»ҶиҸҢе°әеҜёпјҲдёҖж ·е№іеёёдёә 1пҪһ2 Ојmпјүзҡ„еӨ–иІҢгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеӣ жӯӨ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖе…үиҜұеҜје‘ЁжңҹжҖ§иЎЁ йқўзә№зҗҶз»“жһ„еҸҜд»ҘйҖҡиҝҮж”№е–„й’ӣеҗҲйҮ‘еӨ–иІҢзҡ„ж¶Ұж№ҝи§’е’ҢзІ— зіҷеәҰйҷҚдҪҺз»ҶиҸҢзҡ„й»Ҹиөһи®ёеўһж®–гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз»јдёҠжүҖиҝ°�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡеҗҺй’ӣеҸҠй’ӣеҗҲйҮ‘еӨ–иІҢз»“жһ„ е…ідәҺй•Ңжұ°з»ҶиҸҢзҡ„й»Ҹйҷ„дё»иҰҒеҢ…жӢ¬дёӨж–№йқўпјҡдёҖжҳҜйҖҡиҝҮжһ„ е»әе…·жңүзү№еҫҒе°әеҜёе°ҸдәҺз»ҶиҸҢе°әеҜёе’Ңе…·жңүеҫҲжҳҜиҮҙеҜҶзҡ„зү№ еҫҒеӨ–иІҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢй•Ңжұ°з»ҶиҸҢдёҺеӨ–иІҢзҡ„жҺҘи§Ұйқўз§Ҝ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠ‘еҲ¶з»ҶиҸҢзҡ„е®ҡ жӨҚжҲ–еҲәз ҙз»ҶиҸҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠөиҫҫй•Ңжұ°з»ҶиҸҢж»һз•ҷзҡ„зӣ®зҡ„�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣдәҢжҳҜйҖҡиҝҮ еўһеӨ§еӨ–иІҢзҡ„еҮ№йҷ·ж°ҙе№і�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз»ҶиҸҢж— жі•з©ҝиҝҮеҮ№йҷ·дёҺеӨ–иІҢе»ә з«ӢзЁіеӣәзҡ„жҜ—иҝһ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙз»ҶиҸҢеҸӘиғҪй»Ҹйҷ„еңЁдёӘеҲ«зҡ„е°–з«Ҝ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйҳІ жӯў з”ҹзү©иҶңзҡ„еҪўжҲҗгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
2.3гҖҖжҝҖе…үзҶ”иҰҶжҠ—иҸҢж¶ӮеұӮ
жҝҖе…үзҶ”иҰҶжүӢиүәеҸҜд»ҘеңЁй’ӣеҸҠй’ӣеҗҲйҮ‘еӨ–иІҢзҶ”иҰҶе·®еҲ« зі»з»ҹзҡ„еӣ зҙ �пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж”№е–„й’ӣеҗҲйҮ‘зҡ„жҖ§иғҪгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮзҺ°йҳ¶ж®ө�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖе…үзҶ”иҰҶ жүӢиүәз”ЁдәҺжҸҗй«ҳй’ӣеҸҠй’ӣеҗҲйҮ‘жҠ—иҸҢжҖ§иғҪзҡ„зҶ”иҰҶзі»з»ҹдё»иҰҒ еҢ…жӢ¬з”ҹзү©еҢ»з”ЁйҮ‘еұһиҙЁж–ҷпјҲAg�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢCu�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢNb�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢZn�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢTa зӯү[48]пјүгҖҒз”ҹзү©йҷ¶з“·пјҲHA�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢTiO2 зӯү[49]пјүгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжҝҖе…үзҶ”иҰҶжүӢиүәеҸҜд»Ҙжҳҫи‘—жҸҗ й«ҳй’ӣеҸҠй’ӣеҗҲйҮ‘зҡ„жҠ—иҸҢжҖ§иғҪ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе°Өе…¶жҳҜеҜ№йҮ‘й»„иүІи‘Ўиҗ„зҗғиҸҢ е’ҢеӨ§иӮ жқҶиҸҢзӯүеёёи§Ғзҡ„иҮҙз—…иҸҢжңүиҫғеҘҪзҡ„жҠ‘еҲ¶дҪңз”Ё[50] гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
2.3.1гҖҖAg жҠ—иҸҢж¶ӮеұӮ
Ag е…·жңүи¶…ејәзҡ„жҠ—иҸҢжҖ§�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиў«жҷ®йҒҚеә”з”ЁдәҺе№ҝи°ұжқҖиҸҢ иҙЁж–ҷгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮSHI зӯүеӯҰиҖ…[51] йҖҡиҝҮеҜ№й«ҳзңҹз©әз”өеј§зӮүзҶ”зӮјзҡ„ TiAgеҗҲйҮ‘дёҫиЎҢжҠ—иҸҢжҖ§иҜ•йӘҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸ‘жҳҺпјҡеҗҲйҮ‘зҡ„жҠ—иҸҢжҖ§жҳҜз”ұ дәҺ Ti2Ag е’Ң Ag+зҡ„й…ҚзӣёеҠ©з”Ё�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”жІЎжңүеј•иө·з»ҶиғһжҜ’жҖ§гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮCHENзӯүеӯҰиҖ…[52] еҲ¶жҲҗзҡ„ Ti-Ag еҗҲйҮ‘еңЁз»Ҹз”ұзғӯеӨ„зҪ®жғ©зҪҡеҗҺ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜ№йҮ‘й»„иүІи‘Ўиҗ„зҗғиҸҢзҡ„жҠ‘еҲ¶зҺҮй«ҳиҫҫ 99%гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжү№жіЁпјҡAg зҡ„ еҠ е…ҘеҸҜд»ҘдҪҝеҗҲйҮ‘иҺ·еҫ—иҫғејәдё”зЁіеӣәзҡ„жҠ—иҸҢжҖ§иғҪгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
XUE зӯүеӯҰиҖ… [53] йҖҡиҝҮжҝҖе…үзҶ”иҰҶжүӢиүә еңЁ Ti-20Zr10Nb-4TaеӨ–иІҢжҝҖе…үзҶ”иҰҶ Ag з®”�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз ”з©¶ Ag еҫ®зІ’е…ідәҺй’ӣ еҗҲйҮ‘жҠ—иҸҢжҖ§е’Ңзӣёе®№жҖ§зҡ„еҪұе“Қ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиҜ•йӘҢж•Ҳжһңжү№жіЁпјҡеҪ“жҝҖе…ү еҠҹзҺҮдёә 50 W е’Ң 70 W ж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз»Ҹз”ұеӨ„зҪ®жғ©зҪҡзҡ„еӨ–иІҢе…ідәҺеӨ§иӮ жқҶ иҸҢзҡ„жҠ‘иҸҢзҺҮеҲ’еҲҶжҠөиҫҫ 96.3% е’Ң 98.2%�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…ідәҺйҮ‘й»„иүІи‘Ў иҗ„зҗғиҸҢзҡ„жҠ‘иҸҢзҺҮеқҮжҠөиҫҫ 100%�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”йҡҸзқҖжҝҖе…үеҠҹзҺҮзҡ„еўһ еҠ �пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеӨ–иІҢеҪўжҲҗдәҶй’қеҢ–иҶң�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢзІ—зіҷеәҰеўһеӨ§�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…·жңүдјҳејӮзҡ„иҖҗ дҫөиҡҖжҖ§иғҪе’Ңз”ҹзү©зӣёе®№жҖ§гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮZHANG зӯүеӯҰиҖ…[54] е°Ҷ Ag е’ҢZnO зәізұійў—зІ’жҺәе…ҘзҫҹеҹәзЈ·зҒ°зҹізәізұізІүдҪ“дёӯ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖҡиҝҮжҝҖе…ү зҶ”иҰҶжүӢиүәжІүз§ҜеңЁ TC4 еӨ–иІҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜ№жҝҖе…үзҶ”иҰҶж¶ӮеұӮзҡ„жҠ—иҸҢ
жҖ§иғҪе’ҢйӘЁж•ҙеҗҲжҖ§иғҪдёҫиЎҢз ”з©¶гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз ”з©¶еҸ‘жҳҺпјҡзәізұі Ag е’ҢHA еңЁзҶ”иҰҶеұӮеӨ–иІҢе‘ҲжЈ’зҠ¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж¶ӮеұӮдёҺеҹәдҪ“еӣўз»“дјҳејӮ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжңҖ еӨ§зҶ”ж·ұжҠөиҫҫ 460 Ојm�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж¶ӮеұӮзҡ„жңҖе°Ҹж¶Ұж№ҝи§’зәҰдёә 10.5В°гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ жҝҖе…үзҶ”иҰҶеҸҜд»Ҙе°ҶеӨҚеҗҲж¶ӮеұӮз»ҶеҜҶең°зүўйқ еңЁ TC4 еҹәдҪ“дёҠ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠ‘еҲ¶дәҶ Ag зҰ»еӯҗзҡ„йҮҠж”ҫйҖҹзҺҮ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢзј“и§ЈдәҶй«ҳ Ag жө“еәҰдёӢзҡ„ з»ҶиғһжҜ’жҖ§[55]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж¶ӮеұӮе…·жңүдјҳејӮзҡ„з»ҶиҸҢжҠ—жҖ§гҖҒжҲҗйӘЁе’ҢйӘЁж•ҙ еҗҲиғҪеҠӣгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮMAHARUBIN зӯүеӯҰиҖ…[56] йҖҡиҝҮжҝҖе…үеҠ е·ҘеҮҖжҲҗ еҪўе·Ҙиүәе°Ҷж··ж·ҶеҢҖз§°зҡ„ cp-Ti зІүе’Ң Ag зІүжҺҘзәіеҗҢжӯҘйҖҒзІү ж–№жі•еңЁ cp-Ti еҹәдҪ“дёҠеҲ¶еӨҮ银еҗ«йҮҸпјҲиҙЁйҮҸеҲҶж•°пјүдёә 0.5%пҪһ2.0% зҡ„ Ti-Ag еҗҲйҮ‘�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖҡиҝҮ EDS жЈҖжөӢеҸ‘жҳҺпјҡ
Ag еҢҖз§°ең° жј«иЎҚеңЁеҹәдҪ“дёҠгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮйҖҡиҝҮеҜ№е·®еҲ« Ag еҗ«йҮҸзҡ„иҜ•ж ·дёҫиЎҢйҮ‘ й»„иүІи‘Ўиҗ„зҗғиҸҢе’Ңй“ңз»ҝеҒҮеҚ•иғһиҸҢдёҫиЎҢжҠ—иҸҢжҖ§иҜ•йӘҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠ— иҸҢж•ҲжһңйҡҸ Ag еҗ«йҮҸзҡ„еўһж·»иҖҢеўһејә �пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ еҪ“ Ag еҗ«йҮҸиҫҫ еҲ°1.5% ж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠ—иҸҢзҺҮеҲ’еҲҶжҠөиҫҫ 99.79% е’Ң 99.96%�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”еңЁ Agеҗ«йҮҸиҫғдҪҺж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҜд»ҘеңЁдёҚжҚҹе®із”ҹзү©жҙ»жҖ§зҡ„жқЎд»¶дёӢжңҖе°Ҹ еҢ–з»ҶиҸҢзҶҸжҹ“зҡ„еҚұе®ігҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
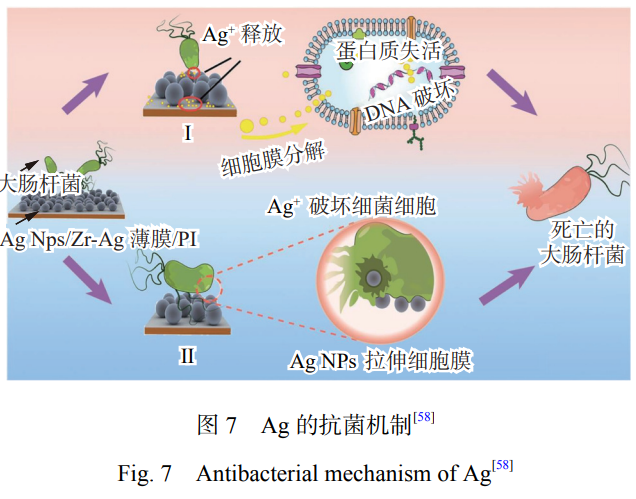
зҺ°еңЁ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…ідәҺ Ag еҜ№еҫ®з”ҹзү©зҡ„жҠ‘еҲ¶е’ҢжқҖдјӨйҖ”еҫ„дё»иҰҒ еҪ’з»“дёәд»ҘдёӢзңӢжі•[57]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶жҠ—иҸҢеҺҹзҗҶеҰӮеӣҫ 7[58] жүҖзӨәгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮAgиғҪеӨҹжҠ—иҸҢзҡ„дё»иҰҒзјҳж•…еҺҹз”ұжҳҜиғҪиў«иҸҢзұ»еҗёйҷ„�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеёҰжӯЈз”өиҚ·зҡ„Ag+иғҪдёҺеёҰиҙҹз”өиҚ·зҡ„еҫ®з”ҹзү©д№Ӣй—ҙзҲҶеҸ‘йқҷз”өеҗёеј•�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҺиҖҢ дҝғдҪҝAg+йҷ„зқҖеңЁз»ҶиғһиҶңдёҠ[59]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз»ҶиҸҢзҡ„з»ҶиғһиҶңеңЁдёҺ AgжҺҘи§ҰеҮ еҲҶй’ҹеҗҺе°ұдјҡиў«е®Ңе…Ёз ҙжҚҹ[60]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҗҢж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢAg иғҪеӨҹдёҺ з»ҶиҸҢзҡ„еҚөзҷҪиҙЁзӣёдә’еӣўз»“�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз ҙжҚҹеҚөзҷҪиҙЁзҡ„з»“жһ„�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйҳ»зўҚз»Ҷ иҸҢзҡ„ж–°йҷҲд»Ји°ў�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҺиҖҢеӨұеҺ»жҙ»жҖ§[61]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮAg+жө“еәҰзҡ„жҸҗй«ҳдјҡ еҜјиҮҙз»Ҷиғһж°§еҢ–еҸҚеә”зҡ„еўһж·»�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҫ®з”ҹзү©з»Ҷиғһж°§еҢ–еә”жҝҖзҡ„ еўһж·»жҳҜ Ag+еј•иө·жҜ’жҖ§дҪңз”Ёзҡ„ж Үи®°гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮз”ұдәҺ Ag иғҪеӨҹеўһиҝӣ з»ҶиғһзҲҶеҸ‘ ROS е’ҢиҮӘз”ұеҹә�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеӣ жӯӨ Ag е…·жңүејәзӣӣзҡ„жҠ—иҸҢгҖҒжҠ—зңҹиҸҢе’ҢжҠ—з—…жҜ’жҙ»жҖ§[62]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҸҜжҳҜ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠ—иҸҢжҖ§иғҪдёҺ银еҗ«йҮҸдёҚ дҝқеӯҳзәҝжҖ§е…ізі»�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ银еҗ«йҮҸиҝҮй«ҳж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ并дёҚдјҡжҳҫи‘—жҸҗй«ҳй’ӣеҗҲ йҮ‘зҡ„жҠ—иҸҢжҖ§иғҪ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҚиҖҢеҸҜиғҪзҲҶеҸ‘з»ҶиғһжҜ’жҖ§[63] гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
2.3.2гҖҖCu жҠ—иҸҢж¶ӮеұӮ
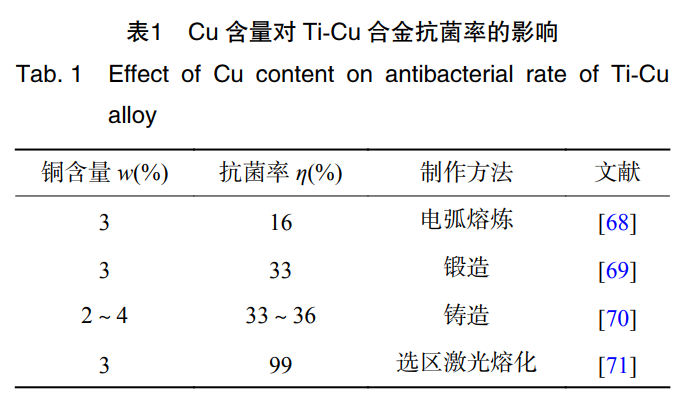
е·®еҲ«зҡ„йҮ‘еұһиҙЁж–ҷжқҖиҸҢиғҪеҠӣд№ҹжңүжүҖе·®еҲ«�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶е·Ёз»ҶжҺ’еәҸ дёәпјҡCu>Fe>Sn>Al>Zn>Co[64]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮCu е…·жңүеўһиҝӣжҲҗйӘЁз»Ҷиғһ еҲҶи§Ј�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиҜұеҜјиЎҖз®Ўз”ҹй•ҝзҡ„дҪңз”ЁгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҗҢж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪңдёәдәәдҪ“еҝ…йңҖзҡ„еҫ®йҮҸ е…ғзҙ �пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжңүйў„йҳІйӘЁиҙЁжқҫж•Јзҡ„дҪңз”Ё[65]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮZHANG зӯүеӯҰиҖ…[66]йҖҡиҝҮжҺҘзәізӯүзҰ»еӯҗзғ§з»“жүӢиүәеҲ¶еӨҮзҡ„ Ti-Cu еҗҲйҮ‘еҜ№еӨ§иӮ жқҶиҸҢе’ҢйҮ‘й»„иүІи‘Ўиҗ„зҗғиҸҢзҡ„жҠ‘еҲ¶зҺҮжҠөиҫҫ 99%гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮжңүз ”з©¶жҠҘйҒ“�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸӘжңү Ti-Cu еҗҲйҮ‘зҡ„ Cu еҗ«йҮҸпјҲиҙЁйҮҸеҲҶж•°пјүеңЁ 5% еҸҠ д»ҘдёҠ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҗҲйҮ‘жүҚе…·жңүжҠ—иҸҢзҺҮ>99% зҡ„жҠ—иҸҢжҖ§иғҪ[67]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиЎЁ 1 дёә еҗҲйҮ‘дёӯ Cu еҗ«йҮҸе·®еҲ«дҪ“зҺ°еҮәзҡ„жҠ—иҸҢжҖ§иғҪ[68-71]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
JI зӯүеӯҰиҖ…[72] жҺҘзәіжҝҖе…үйҖүеҢәзҶ”еҢ–жүӢиүәеҲ¶еӨҮзҡ„ Ti- (3,5,7,10)Cu еҗҲйҮ‘пјҲиҙЁйҮҸеҲҶж•°�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ%пјү�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢTi2Cu зӣёеңЁжҷ¶з•Ңйў„е…Ҳ еҪўж ёе№¶йҳ»жӯўжҷ¶зІ’й•ҝеӨ§�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиғҪеӨҹеҫҲеҘҪзҡ„иө·еҲ°з»ҶеҢ–жҷ¶зІ’зҡ„ дҪңз”ЁгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҗҢж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺжҝҖе…үйҖүеҢәзҶ”еҢ–еҝ«йҖҹеҮқеӣәзҡ„зү№зӮ№�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢTiзҡ„е№іеқҮжҷ¶зІ’е°әеҜёдёә 7.4 Ојm�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиҝңе°ҸдәҺйҖҡдҫӢй“ёйҖ Ti зҡ„жҷ¶ зІ’е°әеҜё�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҝ«йҖҹеҮқеӣәеҜјиҮҙеӨ–иІҢзј©зҹӯиҖҢзҲҶеҸ‘зҡ„з»Ҷе°Ҹеӯ”жҙһ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеўһж·»дәҶз»ҶиҸҢдёҺеҗҲйҮ‘зҡ„жҺҘи§Ұйқўз§Ҝ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠ—иҸҢж•ҲжһңжҳҫзқҖеўһж·»гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҗҲйҮ‘е…·жңүиҫғе°Ҹзҡ„ Cu2+йҮҠж”ҫдё”жңүиҫғй«ҳзҡ„жҠ—иҸҢзҺҮгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮTi-CuеҗҲйҮ‘дёҺз»ҶиҸҢз»ҶиғһиҶңзҡ„зӣҙжҺҘзӣёдә’дҪңз”ЁеҜјиҮҙиҶңзҡ„жё—йҖҸжҖ§ еўһејә�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз»ҶиҸҢе…Ғи®ё Cu2+иҝӣе…Ҙз»ҶиғһеҶ…�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеј•иө·жҺҘи§ҰжқҖиҸҢ[73]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ з»Ҹз”ұжҝҖе…үйҖүеҢәзҶ”еҢ–еҪўжҲҗзҡ„ Ti-3Cu еҗҲйҮ‘зҡ„жҠ—иҸҢзҺҮзӣёе…ідәҺзӣёеҗҢеӣ зҙ зҡ„й“ёйҖ еҗҲйҮ‘�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠ—иҸҢзҺҮжҸҗй«ҳзәҰ 70%гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
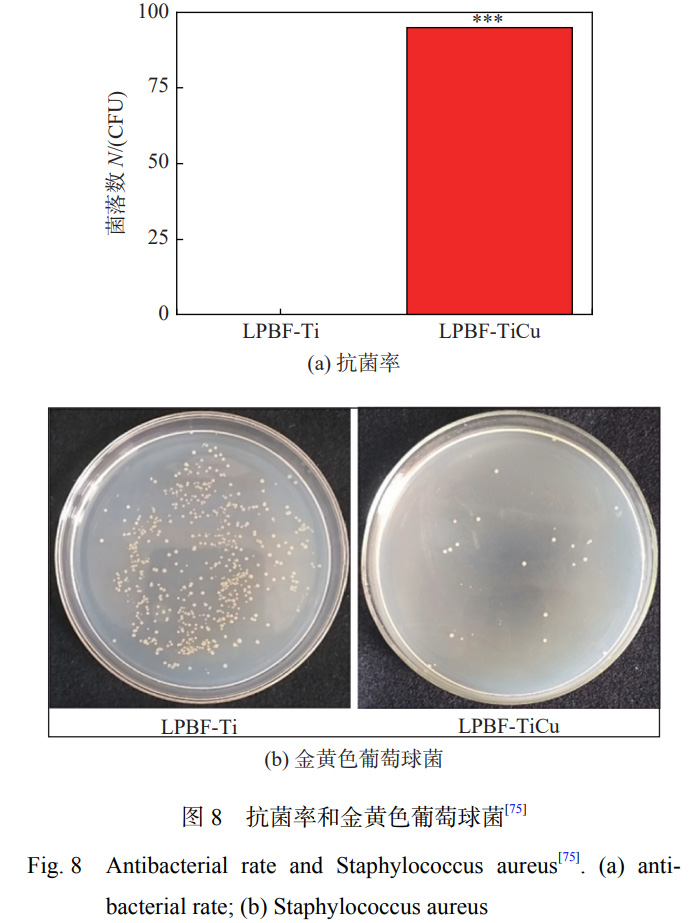
HOU зӯүеӯҰиҖ…[74] йҖҡиҝҮжҝҖе…үзҶ”иҰҶжүӢиүәеңЁ TC4 еӨ–иІҢеҺҹ дҪҚеҲ¶еӨҮжҺәжқӮ Cu йў—зІ’зҡ„ Ca-Si еҹәж¶ӮеұӮ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз ”з©¶жү№жіЁпјҡжҝҖе…үеӨ„зҪ®жғ©зҪҡеҗҺеҺҹдҪҚеӨ©з”ҹдәҶ Ca2SiO4�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢCaTiO3 е’Ң Cu2O�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢж¶ӮеұӮиЎЁ зҺ°еҮәдјҳејӮзҡ„иҖҗзЈЁжҖ§е’Ңж¶Ұж№ҝжҖ§�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣеҪ“ Cu еҗ«йҮҸжҠөиҫҫ 15%ж—¶�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеӨҚеҗҲж¶ӮеұӮе…·жңүеҜ№еӨ§иӮ жқҶиҸҢжңҖй«ҳзҡ„жҠ—иҸҢжҙ»жҖ§гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮLIU зӯү еӯҰиҖ…[75] дҪҝз”ЁжҝҖе…үзІүжң«еәҠзҶ”еҗҲпјҲLPBFпјүжүӢиүәеңЁзәҜй’ӣеҹәдҪ“ дёҠеҲ¶еӨҮжҠ—иҸҢ Ti-Cu еҗҲйҮ‘пјҲLPBF-TiCuпјү�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖе…үеҝ«йҖҹеҠ зғӯ е’ҢеҶ·еҚҙзҡ„дјҳзӮ№зӣёе…ідәҺеҸӨжқҝиҰҒйўҶеҲ¶дҪңзҡ„ Ti-CuеҗҲйҮ‘�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдјҡ дҪҝ Ti еҗҲйҮ‘еҪўжҲҗиҫғеӨҡзҡ„й’ҲзҠ¶й©¬ж°ҸдҪ“пјҲОұвҖІ-Tiпјү�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺе…¶е…· жңүиҫғдҪҺзҡ„иғҪйҮҸзҠ¶жҖҒ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдјҡеҮҸзј“й’ӣеҗҲйҮ‘зҡ„дҫөиҡҖ[76]гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮCu зҡ„ еҠ е…Ҙж”№е–„дәҶ LPBF-TiCu еҗҲйҮ‘дёӯ马ж°ҸдҪ“зӣёеҸҳж—¶еҪўзҠ¶еә” еҸҳзҡ„иҮӘйЎәеә”жҖ§�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢй•Ңжұ°дәҶдҪҚй”ҷеңЁжҷ¶з•Ңзҡ„зҫӨйӣҶгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮLPBFTiCuеҗҲйҮ‘еҸҜд»Ҙжҳҫи‘—еўһиҝӣз»Ҷиғһзҡ„еўһж®–�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҗҲйҮ‘еӨ–иІҢдёҠзҡ„ з»Ҷиғһе…·жңүжӣҙеӨҡзҡ„дјӘи¶і�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ҹзү©зӣёе®№жҖ§дјҳејӮ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜ№йҮ‘й»„иүІи‘Ў иҗ„зҗғиҸҢзҡ„жҠ‘еҲ¶зҺҮжҠөиҫҫ 94.81%�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠ—иҸҢж•ҲжһңеҰӮеӣҫ 8 жүҖзӨәгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
зҺ°еңЁ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…ідәҺжҝҖе…үзҶ”иҰҶеҗ« Cu ж¶ӮеұӮеӨҡз”ЁдәҺж”№еҸҳйҮ‘еұһ зҡ„иҖҗзЈЁжҖ§е’ҢиҖҗдҫөиҡҖжҖ§[77 ? 78]�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢе…ідәҺжҺҘзәіжҝҖе…үзҶ”иҰҶж–№жі•еј•е…Ҙ Cu жҸҗй«ҳжӨҚе…Ҙзү©жҠ—иҸҢжҖ§иғҪзҡ„з ”з©¶иҫғе°‘гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮзҺ°йҳ¶ж®өе…і дәҺ Cu2+зҡ„жқҖиҸҢжңәзҗҶдё»иҰҒиҜ йҮҠдёәеҗ«й“ңзҡ„жҠ—иҸҢйҮ‘еұһиҙЁж–ҷ еңЁжә¶ж¶ІжҲ–дҪ“ж¶Іжғ…еҪўдёӢжә¶еҮәдјҡйҮҠж”ҫеёҰжӯЈз”өзҡ„ Cu2+зҰ»еӯҗ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢиҖҢз»ҶиҸҢзҡ„з”ҹзү©иҶңйҖҡеёёеёҰиҙҹз”өиҚ·�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢдәҢиҖ…д№Ӣй—ҙдјҡзҲҶеҸ‘еҗё йҷ„дҪңз”Ё�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҺиҖҢеҜјиҮҙз»ҶиғһиҶңдёҠзҡ„з”өиҚ·жј«иЎҚдёҚеҢҖз§°�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз»ҶиҸҢ еҪўжҖҒеңЁдёҚеҢҖз§°зҡ„еә“д»‘еҠӣдҪңз”ЁдёӢзҲҶеҸ‘еҸҳеҪў�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢз»ҶиғһиҶңзҡ„ жё—йҖҸжҖ§ж”№еҸҳ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжңҖз»ҲйҖ жҲҗз»ҶиҸҢеЈҒе’Ңз»ҶиҸҢиҶңзҡ„з ҙзўҺ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙ з»ҶиғһиҙЁзҡ„жә¶еҮә�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҺиҖҢжқҖжӯ»з»ҶиҸҢ[79] гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
3гҖҒз«ЈдәӢиҜӯ
пјҲ1пјүжҝҖе…үеӨ–иІҢж”№жҖ§иҜұеҜјй’ӣеҗҲйҮ‘зҲҶеҸ‘жҠ—иҸҢж¶ӮеұӮзҡ„и°ғ жҺ§жңәзҗҶе°ҡдёҚжҳҺзЎ®�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҘеҸҠжҖҺж ·жҸҗеҚҮжҠ—иҸҢж¶ӮеұӮеҲ¶йҖ жүӢиүә зҡ„еҮҶзЎ®жҖ§�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеўһиҝӣжҠ—иҸҢжҖ§е’Ңз”ҹзү©зӣёе®№жҖ§и¶ҠеҸ‘еҚҸи°ғ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҳҜзҺ° йҳ¶ж®өй’ӣеҗҲйҮ‘жҝҖе…үеӨ–иІҢж”№жҖ§зҡ„з ”з©¶йҮҚзӮ№гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
пјҲ2пјүиҷҪ然 Ag�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢCu зӯүжҠ—иҸҢе…ғзҙ зҡ„жҠ—иҸҢжҖ§е·Із»ҸиҺ·еҫ— йӘҢиҜҒгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеҸҜжҳҜ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢзҺ°еңЁе…ідәҺйҮ‘еұһзҰ»еӯҗзҡ„жҠ—иҸҢжңәеҲ¶еҸҠз»Ҷиғһ жҜ’жҖ§жңәеҲ¶зҡ„з ”з©¶е°ҡдёҚжҳҺзЎ®гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеІӮи®әжҳҜйҖҡиҝҮжһ„е»әеҗ«жңүжҠ— иҸҢе…ғзҙ зҡ„жҠ—иҸҢж¶ӮеұӮз…§ж—§еҗҲйҮ‘еҢ–еӨ„зҪ®жғ©зҪҡ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢйғҪйңҖиҰҒеҢ…з®ЎжӨҚ е…Ҙзү©зҡ„жҒ’д№…ж— е®іжҖ§гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮеӣ жӯӨ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҜд»ҘеңЁеҢ…з®ЎжҠ—иҸҢе…ғзҙ зҡ„ жңҖе°Ҹж·»еҠ йҮҸдёӢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҗҢж—¶еҠ е…ҘеӨҡз§Қеҫ®йҮҸжҠ—иҸҢе…ғзҙ гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
пјҲ3пјүе…ідәҺй’ӣеҸҠй’ӣеҗҲйҮ‘зҡ„з”ҹй•ҝ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢд»Қ然йңҖиҰҒеҜ№еј•еҸ‘зӮҺз—Ү е’Ңз»ҶиҸҢзҶҸжҹ“ж–№йқўжҠ•е…ҘеӨ§е®—з ”з©¶гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮй’ӣеҗҲйҮ‘зҡ„жӨҚе…ҘиҰҒеңЁ еҢ…з®ЎеҜ№дәәдҪ“з»„з»ҮжҒ’д№…ж— е®ізҡ„жқЎд»¶дёӢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжһ„е»әзЁіеӣәдё”еӨҡ еҠҹж•Ҳзҡ„еӨҚеҗҲж¶ӮеұӮд»ҘзҹҘи¶ізҺ°е®һеә”з”Ёдёӯзҡ„еӨҡз§ҚйңҖжұӮ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢжҳҜ й’ӣеҸҠй’ӣеҗҲйҮ‘еңЁз”ҹзү©еҢ»з”ЁйўҶеҹҹдёӯжңӘжқҘз ”з©¶зҡ„дё»иҰҒеҒҸеҗ‘гҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
еҸӮиҖғж–ҮзҢ®
[1]vPOU P, RIVEIRO A, DEL VAL J, et al. Laser surface texturing of titanium for bioengineering applications[J].Procedia Manufacturing, 2017, 13: 694 ? 701.
[2]DU PLOOY R, AKINLABI E T. Analysis of laser cladding of titanium alloy[J]. Materials Today:Proceedings, 2018, 5(9): 19594 ? 19603.
пј»3пјҪеӯҷеЈ®, зҺӢдјҹ, зҺӢжҲҗ, зӯү. й’ӣеҗҲйҮ‘еӨ–иІҢжҝҖе…үзҶ”иҰҶиҖҗзЈЁе’ҢиҮӘж¶Ұж»‘ ж¶ӮеұӮзҡ„з ”з©¶еёҢжңӣ [J]. иҙЁж–ҷ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣ, 2023,56(1): 107 ? 120.
SUN Zhuang, WANG Wei, WANG Cheng, et al. Research progress of wear-resistant and self-lubrication coatings prepared on titanium alloy surface by laser cladding[J]. Material Protection, 2023, 56(1): 107 ? 120.
пј»4пјҪLIU S Y, SHIN Y C. Additive manufacturing of Ti6Al4V alloy: A review[J]. Materials &Design, 2019, 164: 107552.
пј»5пјҪ еҗҙиҖҖдҪі, еј жҮӢиҫҫ, д»ҳж°ёејә, зӯү. еҗ« Ag зЎ¬иҙЁж¶ӮеұӮзҡ„з»“жһ„еҸҠе…¶ж‘©ж“ҰдҫөиҡҖдёҺжҠ—иҸҢзү№еҫҒзҡ„з ”з©¶еёҢжңӣ [J]. еӨ–иІҢжүӢиүә, 2021, 50(1): 94 ? 106, 161.
WU Yaojia, ZHANG Maoda, FU Yongqiang, et al. Research progress in structure, tribocorrosion and antibacterial properties of Ag-containing hard coatings[J]. Surface Technology, 2021, 50(1): 94 ? 106, 161.
пј»6пјҪAPAZA-BEDOYA K, TARCE M, BENFATTI C A M, et al. Synergistic interactions between corrosion and wear at titanium-based dental implant connections: A scoping review[J]. Journal of Periodontal Research, 2017, 52(6): 946 ? 954.
пј»7пјҪCHAN C W, CARSON L, SMITH G C, et al. Enhancing the antibacterial performance of orthopaedic implant materials by fibre laser surface engineering[J]. Applied Surface Science,2017, 404: 67 ? 81.
пј»8пјҪZIMMERLI W. Clinical presentation and treatment of orthopaedic implant-associated infection[J]. Journal of Internal Medicine, 2014, 276(2): 111 ? 119.
пј»9пјҪCAMPOCCIA D, MONTANARO L, ARCIOLA C R. The significance of infection related to orthopedic devices and issues of antibiotic resistance[J]. Biomaterials, 2006, 27(11): 2331 ?2339.
пј»10пјҪFLEMMING H C, VAN HULLEBUSCH E D, NEU T R. The biofilm matrix: multitasking in a shared space[J].Nature Reviews Microbiology, 2023, 21(2): 70 ? 86.
пј»11пјҪиҢғз«һдёҖ, 马иҝ…, жқҺдјҹ, зӯү. еҢ»з”Ёй’ӣеҗҲйҮ‘еӨ–иІҢж”№жҖ§жүӢиүәз ”з©¶иҝӣ еұ• [J]. еҠҹж•ҲиҙЁж–ҷ, 2022, 53(7): 7027 ? 7039.
FAN Jingyi, MA Xun, LI Wei, et al. Research progress of surface modification technology of biomedical titanium alloy[J]. Journal of Functional Materials, 2022, 53(7): 7027 ? 7039.
пј»12пјҪNIE BinвҖҷen, LONG Teng, AO Haiyong, et al. Covalent immobilization of enoxacin onto titanium implant surfaces for inhibiting multiple bacterial species infection and in vivo methicillin-resistant staphylococcus aureus infection prophylaxis[J]. Antimicrobial Agents and Chemotherapy, 2016, 60(1): e01766 ? 16.
пј»13пјҪALT V, BITSCHNAU A, ?STERLING J, et al. The effects of combined gentamicin-hydroxyapatite coating for cementless joint prostheses on the reduction of infection rates in a rabbit infection prophylaxis model[J].Biomaterials, 2006, 27: 4627 ? 4634.
пј»14пјҪDONG Yaning, LIU Li, SUN Jin, et al. Phosphonate/quaternary ammonium copolymers as high-efficiency antibacterial coating for metallic substrates[J]. Journal of Materials Chemistry B, 2021, 9(39): 8321 ? 8329.
пј»15пјҪ з§ҰжҖқж°‘. еҹәдәҺз”ҹзү©иў«иҶңзҡ„иҖҗиҚҜжҖ§жҠ—иҸҢеүӮз ”з©¶е’Ңе·ҘзЁӢж–°жқҗ ж–ҷжҺўзҙў [D]. еҢ—дә¬: дёӯеӣҪ科еӯҰйҷўеӨ§еӯҰ,2022.
QIN Simin. Research on drug-resistant antibacterial agents and exploration of new engineering materials based on biofilms[D]. Beijing, China: University of Chinese Academy of Sciences, 2022.
пј»16пјҪзҺӢдёңз”ҹ, з”°е®—еҶӣ, жІҲзҗҶиҫҫ, зӯү. жҝҖе…үзҶ”иҰҶжүӢиүәз ”з©¶зҺ°зҠ¶еҸҠе…¶ з”ҹй•ҝ [J]. еә”з”ЁжҝҖе…ү, 2012, 32(6):538 ? 544.
WANG Dongsheng, TIAN Zongjun, SHEN Lida, et al. Research status and development of laser cladding technology[J]. Applied Laser, 2012, 32(6): 538 ? 544.
пј»17пјҪеҙ”жҢҜй“Һ, жңұ家民, е§ңиҫү, зӯү. Ti еҸҠй’ӣеҗҲйҮ‘еӨ–иІҢж”№жҖ§еңЁз”ҹзү©еҢ» з”ЁйўҶеҹҹзҡ„з ”з©¶еёҢжңӣ [J]. йҮ‘еұһеӯҰжҠҘ,2022, 58(7): 837 ? 856.
CUI Zhenduo, ZHU Jiamin, JIANG Hui, et al. Research progress of the surface modification of titanium and titanium alloys for biomedical application[J]. Acta Metallurgica Sinica, 2022,58(7): 837 ? 856.
пј»18пјҪSIDDIQUI A A, DUBEY A K. Recent trends in laser cladding and surface alloying[J]. Optics & Laser Technology, 2021, 134: 106619.
пј»19пјҪJU Jiang, ZAN Rui, SHEN Zhao, et al. Remarkable bioactivity, bio-tribological, antibacterial, and anti-corrosion properties in a Ti6Al4V-xCu alloy by laser powder bed fusion for superior biomedical implant applications[J].Chemical Engineering Journal, 2023, 471:144656.
пј»20пјҪеј ж°ёеә·, е‘Ёе»әеҝ , еҸ¶дјҡйңһ, зӯү. жҝҖе…үеҠ е·ҘжүӢиүә [M]. еҢ—дә¬: еҢ– еӯҰе·ҘдёҡеҮәд№ҰзӨҫ, 2006.
ZHANG Yongkang, ZHOU Jianzhong, YE Huixia, et al. Laser processing technology [M]. Beijing,China: Chemical Industry Press, 2006.
пј»21пјҪSYPNIEWSKA J, SZKODO M. Influence of laser modification on the surface character of biomaterials: Titanium and its alloys-A review[J]. Coatings, 2022, 12: 1371.
пј»22пјҪLIU Zhifang, NIU Tong, LEI Yaxi, et al. Metal surface wettability modification by nanosecond laser surface texturing: A review[J]. Biosurface and Biotribology, 2022(2): 95 ?120.
пј»23пјҪXU Yong, LIU Wei, ZHANG Gangqiang, et al. Friction stability and cellular behaviors on laser textured Ti6Al4V alloy implants with bioinspired micro-overlapping structures[J].Journal of the Mechanical Behavior of Biomedical Materials, 2020, 109: 103823.
пј»24пјҪWANG Xinlin, LEI Lei, YU Han. A review on microstructural features and mechanical properties of wheels/rails cladded by laser cladding[J]. Micromachines, 2021, 12(2): 152.
пј»25пјҪ ZHANG Yifu, ZHANG Hua, ZHU Zhengqiang, et al.Microstructure, properties and first principles calculation of titanium alloy/steel by Nd: YAG laser self-fluxing welding[J]. China Welding, 2018, 27(3): 1 ? 10.
пј»26пјҪе‘ЁдҪіиүҜ, иҲ’еҮӨиҝң, иөөжҙӘиҝҗ, зӯү. жҝҖе…үзҶ”иҰҶеңЁ AlN йҷ¶з“·еӨ–иІҢеҲ¶ еӨҮй“ңеҹәйҮ‘еұһиҰҶеұӮзјәйҷ·еү–жһҗеҸҠжҺ§еҲ¶ [J].з„ҠжҺҘеӯҰжҠҘ, 2019, 40(11): 133 ? 138.
ZHOU Jialiang, SHU Fengyuan, ZHAO Hongyun, et al. Analysis and control of defects in preparing copper-based metal coatings on AlN ceramic surface by laser cladding[J].Transactions of the China Welding Institution, 2019, 40(11): 133 ? 138.
пј»27пјҪиўҒеәҶйҫҷ, еҶҜж—ӯдёң, жӣ№жҷ¶жҷ¶, зӯү. жҝҖе…үзҶ”иҰҶжүӢиүәз ”з©¶еёҢжңӣ [J].иҙЁж–ҷеҜјжҠҘ, 2010, 24(3): 112 ? 116.
YUAN Qinglong, FENG Xudong, CAO Jingjing, et al. Research progress of laser cladding technology[J]. Materials Reports, 2010, 24(3): 112 ? 116.
пј»28пјҪзҺӢеһҡ. е–·е°„з”өжІүз§ҜеүҚеӨ„зҪ®жғ©зҪҡзҡ„жҝҖе…үеӨ–иІҢеӨ„зҪ®жғ©зҪҡиҰҒйўҶдёҺиҜ•йӘҢз ” 究 [D]. еҚ—дә¬: еҚ—дә¬иҲӘз©әиҲӘеӨ©еӨ§еӯҰ, 2019.
WANG Yao. Experimental Study on Laser surface treatment method of pre-electrodeposition[D]. Nanjing, China: Nanjing University of Aeronautics and Astronautics, 2019.
пј»29пјҪжһ—еҹәиҫү, еҲҳеҫ·й‘«, жқҺиҖҖ, зӯү. жҝҖе…үеҗҲйҮ‘еҢ–жүӢиүәеңЁеӨ–иІҢж”№жҖ§дёӯ зҡ„еә”з”Ёз ”з©¶еёҢжңӣ [J]. зғӯеҠ е·Ҙе·Ҙиүә,2020, 49(8): 13 ? 16.
LIN Jihui, LIU Dexin, LI Yao, et al. Research Progress in application of laser alloying technology in surface modification[J]. Hot Working Technology, 2020, 49(8): 13 ? 16.
пј»30пјҪQIAO Q, CRISTINO V A M, TAM L M, et al. Characterization of laser surface-alloyed Ti-Ni-Ag coatings and evaluation of their corrosion and antibacterial performance[J]. Surface and Coatings Technology, 2023, 474: 130119.
пј»31пјҪCHAN C W, LEE S, SMITH G, et al. Enhancement of wear and corrosion resistance of beta titanium alloy by laser gas alloying with nitrogen[J]. Applied Surface Science, 2016, 367: 80 ?90.
SANTOS E C, MORITA M, SHIOMI M, et al. Laser gas nitriding of pure titanium using CW and pulsed Nd: YAG lasers[J]. Surface and Coatings Technology, 2006, 201: 1635 ? 1642.
пј»32пјҪйӮ№жҙҒ,йҷҲжҙҒ, иғЎж»Ё. TiN ж¶ӮеұӮеҜ№зүҷ科й’ҙ铬еҗҲйҮ‘жҠ—иҸҢдҫөиҡҖжҖ§иғҪ зҡ„еҪұе“Қ [J]. дёҠжө·�пјҹпјҹ�пјҹ�пјҹ�пјҹпјҹи°ҮзҒ°зӘ–, 2010, 19(2): 173 ? 177.
пј»33пјҪ ZOU Jie, CHEN Jie, HU Bin. Effect of titanium nitride coating on bacterial corrosion resistance of dental Co-Cr alloy[J]. Shanghai Journal of Stomatology, 2010, 19(2): 173 ? 177.
пј»34пјҪ DONAGHY C L, MCFADDEN R, KELAINI S, et al. Creating an antibacterial surface on beta TNZT alloys for hip implant applications by laser nitriding[J]. Optics & Laser Technology,2020, 121: 105793.
пј»35пјҪиӮ–еҝҶжҘ , д№”еІ©ж¬Ј, жқҺжңҲжҳҺ, зӯү. еҢ»з”Ёй’ӣеҸҠй’ӣеҗҲйҮ‘еӨ–иІҢж”№жҖ§жҠҖ жңҜзҡ„з ”з©¶еёҢжңӣ [J]. иҙЁж–ҷеҜјжҠҘ, 2019,33(Z2): 336 ? 342.
XIAO Yinan, QIAO Yanxin, LI Yueming, et al. Research development of surface modification technology of biomedical titanium and titanium alloy[J]. Materials Reports, 2019, 33(Z2): 336 ?342.
пј»36пјҪFATHI-HAFSHEJANI P, JOHNSON H, AHMADI Z, et al. Phase-selective and localized TiO2 coating on additive and wrought titanium by a direct laser surface modification approach[J]. ACS Omega, 2020, 5(27): 16744 ? 16751.
пј»37пјҪPARMAR V, KUMAR A, SANKAR M M, et al. Oxidation facilitated antimicrobial ability of laser micro-textured titanium alloy against gram-positive Staphylococcus aureus for biomedical applications[J]. Journal of Laser Applications, 2018, 30(3): 032001.
пј»38пјҪCUNHA A, ELIE A M, PLAWINSKI L, et al. Femtosecond laser surface texturing of titanium as a method to reduce the adhesion of Staphylococcus aureus and biofilm formation[J]. Applied Surface Science, 2016, 360: 485 ? 493.
пј»39пјҪVARIOLA F, YI J H, RICHERT L, et al. Tailoring the surface properties of Ti6Al4V by controlled chemical oxidation[J]. Biomater, 2008, 29(10): 1285 ? 1298.
пј»40пјҪжқҺеҚҺжҷЁ, е‘Ёе№ҝж¶ӣ, йҷҲжў…еі°, зӯү. еҲҶжӯҘж°”дҪ“д»ӢиҙЁдёӢдҪҺеҠҹзҺҮжҝҖе…ү з„ҠжҺҘи–„жқҝзҙ«й“ңжҲҗеҪўеҸҠз»„з»Үе’ҢжҖ§иғҪ [J].з„ҠжҺҘеӯҰжҠҘ, 2020, 41(10): 65 ? 72.
LI Huachen, ZHOU Guangtao, CHEN Meifeng, et al. Research on laser welding formability and microstructure property of copper in stepwise gas medium[J]. Transactions of the China Welding Institution, 2020, 41(10): 65 ? 72.
пј»41пјҪGALLARDO-MORENO A M, PACHA-OLIVENZA M A, SALDA?A L, et al. In vitro biocompatibility and bacterial adhesion of physico-chemically modified Ti6Al4V surface by means of UV irradiation [J]. Acta Biomaterialia, 2009, 5(1): 181 ? 192.
пј»42пјҪMITIK-DINEVA N, WANG J, TRUONG V K, et al. Escherichia coli, Pseudomonas aeruginosa, and Staphylococcus aureus attachment patterns on glass surfaces with nanoscale roughness[J].Current Microbiology, 2009, 58: 268 ? 273.
пј»43пјҪJEYACHANDRAN Y L, NARAYANDASS S K. The effect of thickness of titanium nitride coatings on bacterial adhesion[J]. Trends in Biomaterials and Artificial Organs, 2010, 24(2): 90 ? 93.
пј»44пјҪ GIRALDEZ M J, RESUA C G, LIRA M, et al. ContactLens hydrophobicity and roughness
effects on bacterial adhesion[J]. Optometry and Vision Science, 2010, 87(6): E426 ? E431.
пј»45пјҪPOGODIN S, HASAN J, BAULIN V A, et al. Biophysical model of bacterial cell interactions
with nanopatterned cicada wing surfaces[J]. Biophysical Journal, 2013, 104(4): 835 ? 840.
пј»46пјҪTRUONG V K, LAPOVOK R, ESTRIN Y S, et al. The influence of nano-scale surface roughness
on bacterial adhesion to ultrafine-grained titanium[J]. Biomaterials, 2010, 31(13): 3674 ?
3683.
пј»47пјҪBRAEM A, VAN MELLAERT L, MATTHEYS T, et al. Staphylococcal biofilm growth on smooth and
porous titanium coatings for biomedical applications[J]. Journal of Biomedical Materials
Research Part A, 2014, 102: 215 ? 224.
пј»48пјҪеҸёй“¶иҠі, иғЎиҜӯе©•, еј еҮЎ, зӯү. з”ҹзү©еҗҲжҲҗж°§еҢ–й”Ңзәізұійў—зІ’иҙЁж–ҷ еҸҠе…¶жҠ—иҸҢеә”з”Ё [J]. еҢ–е·ҘеёҢжңӣ, 2023, 42(4): 2013 ? 2023.
SI Yinfang, HU Yujie, ZHANG Fan, et al. Biosynthesis of zinc oxide
nanoparticles and its application to antibacterial[J]. Chemical Industry and Engineering
Progress, 2023, 42(4): 2013 ? 2023.
пј»49пјҪи®ёжҷҙ. з”ҹзү©жҙ»жҖ§йҷ¶з“·еӨҚеҗҲиҙЁж–ҷеҲ¶еӨҮеҸҠе…¶жҠ—иҸҢе’ҢеҶҚз”ҹдҝ®еӨҚ з ”з©¶ [D]. еҢ—дә¬: дёӯеӣҪ科еӯҰйҷўеӨ§еӯҰ, 2021. XU Qing. Preparation of bioactive ceramic composites and its antibacterial activity and regenerative repair effect[D]. Beijing, China: University of Chinese Academy of Sciences,2021.
пј»50пјҪZHOU Yazhou, YANG Juan, HE Tingting, et al. Highly stable and dispersive silver nanoparticle-graphene composites by a simple and low-energy-consuming approach and their antimicrobial activity[J]. Small, 2013, 9(20): 3445 ? 3454.
пј»51пјҪSHI Anqi, ZHU Chenshun, FU Shan, et al. What controls the antibacterial activity of Ti-Ag alloy, Ag ion or Ti2Ag particles?[J]. Materials Science and Engineering: C, 2020, 109:110548.
пј»52пјҪCHEN Mian, YANG Lei, ZHANG Lan, et al. Effect of nano/micro-Ag compound particles on the bio-corrosion, antibacterial properties and cell biocompatibility of Ti-Ag alloys[J].Materials Science and Engineering: C, 2017, 75: 906 ? 917.
пј»53пјҪXUE Xianda, LU Libin, HE Donglei, et al. Antibacterial properties and cytocompatibility of Ti-20Zr-10Nb-4Ta alloy surface with Ag microparticles by laser treatment[J]. Surface and Coatings Technology, 2021, 425: 27716.
пј»54пјҪ ZHANG Yanzhe, LIU Xiangmei, LI Zhaoyang, et al. Nano Ag/ZnO-incorporated hydroxyapatite composite coatings: highly effective infection prevention and excellent osteointegration[J].ACS Applied Materials & Interfaces, 2018, 10(1): 1266 ? 1277.
пј»55пјҪдёҒе©·е©·. еҗ«й“¶зәізұіиҙЁж–ҷзҡ„еҲ¶еӨҮгҖҒжҠ—иҸҢжҖ§иғҪеҸҠз»ҶиғһжҜ’жҖ§з ” 究 [D]. й•ҝжІҷ: ж№–еҚ—еӨ§еӯҰ, 2020.
DING Tingting. Preparation, antibacterial properties and cytotoxicity of silver-containing nanomaterials[D]. Changsha, China: Hunan University, 2020.
пј»56пјҪMAHARUBIN S, HU Y B, SOORIYAARACHCHI D. Laser engineered net shaping of antimicrobial and biocompatible titanium-silver alloys[J]. Materials Science and Engineering: C, 2019, 105:110059.
пј»57пјҪжқҺжіў. еҹәдәҺ银еҹәзәізұіеӨҚеҗҲз”ҹзү©иҙЁж–ҷйқ¶еҗ‘еҚҸеҗҢжҠ—иҸҢз”ЁдәҺйӘЁ зҶҸжҹ“жІ»з–— [D]. дёҠжө·: дёңеҚҺеӨ§еӯҰ, 2022.
LI Bo. Targeted synergistic antibacterial based on silverbased nanocomposite biomaterials for bone infection treatment[D]. Shanghai, China: Donghua University, 2022.
пј»58пјҪSHI Pengyan, SUN Haoliang, ZHANG Haoge, et al. Highly effective antibacterial properties of self-formed Ag nanoparticles/Zr-Ag granular films[J]. Applied Surface Science, 2023, 622: 156929.
пј»59пјҪABBASZADEGAN A, GHAHRAMANI Y, GHOLAMI A, et al. The effect of charge at the surface of silver nanoparticles on antimicrobial activity against gram-positive and gram-negative bacteria: A preliminary study[J]. Journal of Nanomaterials, 2015, 2015: 720654.
пј»60пјҪRAFFI M, HUSSAIN F, BHATTI T M, et al. Antibacterial characterization of silver nanoparticles against E. coli ATCC15224[J]. Journal of Materials Science & Technology, 2008,24(2): 192 ? 196.
пј»61пјҪеј дҝҠж•Ҹ. Ti-Ta-Ag еҗҲйҮ‘зҡ„ж”ҫз”өзӯүзҰ»еӯҗдҪ“зғ§еӣўз»“жҲҗжңәзҗҶеҸҠ е…¶жҖ§иғҪз ”з©¶ [D]. жҳҶжҳҺ: жҳҶжҳҺзҗҶе·ҘеӨ§еӯҰ,2022.
ZHANG Junmin. Study on the synthesis mechanism and properties of Ti-Ta-Ag alloy by spark plasma sintering[D]. Kunming, China: Kunming University of Science and Technology, 2022.
пј»62пјҪKIM S, LEE H S, RYU D, et al. Antibacterial activity of silver-nanoparticles against Staphylococcus aureus and Escherichia coli[J]. Korean Journal of Microbiology & Biotechnology,2011, 39(1): 77 ? 85.
пј»63пјҪFENG Q L, WU J, CHEN G Q, et al. A mechanistic study of the antibacterial effect of silver ions on Escherichia coli and Staphylococcus aureus[J]. Journal
of Biomedical Materials Research, 2000, 52(4): 662 ? 668.
пј»64пјҪзҪ—еЁҹ. зәізұі Ag-Cu еҹәжҠ—иҸҢиҙЁж–ҷзҡ„еҲ¶еӨҮеҸҠе…¶жҖ§иғҪз ”з©¶ [D].жҳҶжҳҺ: жҳҶжҳҺзҗҶе·ҘеӨ§еӯҰ, 2022.
LUO Juan. Preparation and properties of nano Ag-Cu based antibacterial materials[D]. Kunming, China: Kunming University of Science and Technology, 2022.
пј»65пјҪSRIKANT P, REDDY C K, RAM N R. Metallic particulates for preparation of anti-bacterial preservation vassals and their applications-A review[J]. Materials Today:Proceedings, 2019, 18: 440 ? 444.
пј»66пјҪZHANG Erlin, FU Shan, WANG Ruoxian, et al. Role of Cu element in biomedical metal alloy design[J]. Rare Metals, 2019, 38(6): 476 ? 494.
пј»67пјҪZHANG Erlin, LI Shengyi, REN Jing, et al. Effect of extrusion processing on the microstructure, mechanical properties, biocorrosion properties and antibacterial properties of Ti-Cu sintered alloys[J]. Materials Science and Engineering: C, 2016, 69: 760 ? 768.
пј»68пјҪLIU Jie, LI Fangbing, LIU Cong, et al. Effect of Cu content on the antibacterial activity of titanium-copper sintered alloys[J]. Materials Science and Engineering: C, 2014, 35: 392 ? 400.
пј»69пјҪFOWLER L, JANSON O, ENGQVIST H, et al. Antibacterial investigation of titanium-copper alloys using luminescent Staphylococcus epidermidis in a direct contact test[J].Materials Science and Engineering: C, 2019, 97: 707 ? 714.
пј»70пјҪBAO Mianmian, LIU Ying, WANG Xiaoyan, et al. Optimization of mechanical properties, biocorrosion properties and antibacterial properties of wrought Ti-3Cu alloy by heat treatment[J]. Bioactive Materials, 2018, 3(1): 28 ? 38.
пј»71пјҪZHANG Erlin, REN Jing, LI Shengyi, et al. Optimization of mechanical properties, biocorrosion properties and antibacterial properties of as-cast Ti-Cu alloys[J].Biomedical Materials, 2016, 11: 065001.
пј»72пјҪJI Hairui, ZHAO Mingchun, XIE Bin, et al. Corrosion and antibacterial performance of novel selective-laser-melted (SLMed) Ti-xCu biomedical alloys[J]. Journal of Alloys and Compounds, 2021, 8644: 158415.
пј»73пјҪPENG Cong, ZHANG Shuyuan, SUN Ziqing, et al. Effect of annealing temperature on mechanical and antibacterial properties of Cu-bearing titanium alloy and its preliminary study of antibacterial mechanism[J]. Materials Science and Engineering: C, 2018, 93: 495 ? 504.
пј»74пјҪHOU Baoping, YANG Zhao, YANG Yuling, et al. In vitro bioactivity, tribological property, and antibacterial ability of Ca-Si-based coatings doped with cu particles in-situ fabricated by laser cladding[J]. Applied Physics A, 2018, 124: 256.
пј»75пјҪLIU Hui, SHI Lizhen, LIU Huan, et al. Corrosion behavior of laser powder bed fusion prepared antibacterial Cu-bearing titanium alloy[J]. Materials Letters, 2023, 331: 133496.
пј»76пјҪKASCHEL F R, KEAVENEY S, DOWLING D P. Comparison between continuous and modulated wave laser emission modes for the selective laser melting of Ti-6Al-4V: Dimensional accuracy,microstructure and mechanical behaviour[J]. Additive Manufacturing, 2022, 55: 102825.
пј»77пјҪи°ўеҸ‘еӢӨ, дҪ•й№Ҹ, еҗҙеҗ‘жё…, зӯү. й’ӣеҗҲйҮ‘еӨ–иІҢжҝҖе…үзҶ”иҰҶжүӢиүәзҡ„з ” 究еҸҠеұ•жңӣ [J]. жңүж•°йҮ‘еұһиҙЁж–ҷдёҺе·ҘзЁӢ,2022, 51(4): 1514 ? 1524.
XIE Fanqin, HE Peng, WU Xiangqing, et al. Research and prospect of laser cladding technology on titanium alloy surface[J]. Rare Metal Materials and Engineering,
2022, 51(4): 1514 ? 1524.
пј»78пјҪй»„ж№ҳж№ҳ. зўій’ўеӨ–иІҢжҝҖе…үзҶ”иҰҶй“қйқ’й“ңеҗҲйҮ‘з»„з»Үе’ҢжҖ§иғҪз ”з©¶[D]. дёҠжө·: дёҠжө·дәӨйҖҡеӨ§еӯҰ, 2019.
HUANG Xiangxiang. Microstructure and properties of laser cladded aluminum bronze coating on carbon steel[D]. Shanghai, China: Shanghai Jiao Tong University, 2019.
пј»79пјҪзҺӢдәҡиҝӘ. еҹәдәҺйҳізҰ»еӯҗ-ПҖ дҪңз”Ёзҡ„й“ңеӨҚеҗҲзү©зҡ„жҠ—иҸҢжҖ§иғҪдёҺжңә зҗҶз ”з©¶ [D]. еҢ—дә¬: дёӯеӣҪ科еӯҰйҷўеӨ§еӯҰ,2020.
WANG Yadi. Copper complexes based on cation-ПҖ interaction: Preparation characterization and antimicrobial activities[D]. Beijing, China: University of Chinese Academy of Sciences,2020.
第дёҖдҪңиҖ…пјҡгҖҖ马жҢҜ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҚҡеЈ«�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеүҜж•ҷжҺҲ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣдё»иҰҒд»ҺдәӢеҢ»з”Ёй’ӣеҗҲйҮ‘еӨ–иІҢ ж”№жҖ§зҡ„з§‘з ”е’Ңж•ҷеӯҰдәӢжғ…�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣе·ІжҸӯжҷ“и®әж–Ү 20 дҪҷзҜҮ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣjmsdxmz@163.comгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮйҖҡи®ҜдҪңиҖ…пјҡгҖҖзүҹз«Ӣе©·�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеҚҡеЈ«�пјҢ�пјҢ�пјҢ�пјҢ�пјҢ�пјҢеүҜж•ҷжҺҲ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣдё»иҰҒд»ҺдәӢеҢ»з”Ёз”ҹзү©иҙЁж–ҷ з ”з©¶�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣmuliting@163.comгҖӮгҖӮгҖӮ�гҖӮ�гҖӮгҖӮ�гҖӮгҖӮ
зӣёе…ій“ҫжҺҘ
















